题目内容
3.下列说法不正确的是( )| A. | 氯气、二氧化氯、臭氧都可用于自来水的消毒 | |
| B. | 氯水、漂白液、漂白粉的溶液都能是有色布条褪色 | |
| C. | 某溶液加入硝酸银溶液产生白色沉淀,加入盐酸沉淀不消失,该溶液一定含Cl- | |
| D. | 氯气在化学工业中可用来制取高纯度的硅、锗、钛 |
分析 A、氯气和水反应生成具有强氧化性的次氯酸,可用于杀菌消毒,二氧化氯中氯的化合价为+4价,具有较强的氧化性,臭氧有强氧化性;
B、氯水、漂白液、漂白粉的溶液中都含有能使有色布条褪色的物质次氯酸;
C、溶液中加入硝酸银溶于生成白色沉淀不一定是氯化银沉淀,再加入盐酸溶液中含有氯离子,可以发生沉淀转化生成氯化银沉淀;
D、根据制取高纯硅、锗和钛反应原理来分析,粗硅、锗和钛先与氯气反应制得SiCl4、GeCl4、TiCl4,然后再使SiCl4、GeCl4、TiCl4分别与氢气反应即可制得.
解答 解:A、Cl2+H2O=HCl+HClO,氯气与水反应生成次氯酸,HClO具有强氧化性,可用于杀菌消毒,二氧化氯中氯的化合价为+4价,不稳定,易转变为-1价,从而体现较强的氧化性,可用于自来水的杀菌消毒,臭氧有强氧化性,能杀菌消毒,故A正确;
B、氯水中含有HClO,具有漂白作用,漂白粉的有效成分为次氯酸钙,能生成具有漂白性的HClO,可使红色布条褪色,次氯酸钠溶液能生成具有漂白性的HClO,可使红色布条褪色,故B正确;
C、溶液中加入硝酸银溶于生成白色沉淀不一定是氯化银沉淀,再加入盐酸溶液中含有氯离子,可以发生沉淀转化生成氯化银沉淀,氯化银不溶于酸,所以溶于不一定含氯离子,故C错误;
D.制取高纯硅、锗和钛时,将粗硅、锗和钛先与氯气反应制得SiCl4、GeCl4、TiCl4,然后再使SiCl4、GeCl4、TiCl4分别与氢气反应即可制的高纯的硅、锗和钛,故D正确.
故选C.
点评 本题考查了物质性质的分析应用,主要是物质化学性质和反应实质的理解应用,掌握基础是解题关键,题目较简单.

练习册系列答案
 黄冈天天练口算题卡系列答案
黄冈天天练口算题卡系列答案
相关题目
14.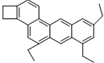 如图是一种形状酷似一条小狗的有机物,化学家Tim Rickard将其取名为“doggycene”,有关doggycene的说法正确的是 ( )
如图是一种形状酷似一条小狗的有机物,化学家Tim Rickard将其取名为“doggycene”,有关doggycene的说法正确的是 ( )
 如图是一种形状酷似一条小狗的有机物,化学家Tim Rickard将其取名为“doggycene”,有关doggycene的说法正确的是 ( )
如图是一种形状酷似一条小狗的有机物,化学家Tim Rickard将其取名为“doggycene”,有关doggycene的说法正确的是 ( )| A. | 该分子中所有碳原子可能处于同一平面 | |
| B. | doggycene的分子式为:C26H30 | |
| C. | 1mol该物质在氧气中完全燃烧生成CO2和水的物质的量之比为1:1 | |
| D. | 该物质常温为气态. |
8.下列有关物质的性质描述不符合事实的是( )
| A. | 氧化铝是冶炼金属铝的原料,由于它熔点高,也是一种较好的耐火材料 | |
| B. | 在混有少量泥沙浑浊水两只试管分别加入少量明矾、硫酸铁溶液,水变得清澈 | |
| C. | 纯净的SiO2是现代光学及光纤制品的基本原料,也是人类将太阳能转化电能的常用材料 | |
| D. | 酸雨是由大气中SO2、NO2溶于雨水形成的 |
15.在恒温恒容的容器中进行反应N2(g)+3H2(g)$?_{催化剂}^{高温、高压}$2NH3(g),若氮气浓度由0.1mol•L-1降到0.06mol•L-1需2s,那么由0.06mol•L-1降到0.024mol•L-1需要的反应时间为( )
| A. | 等于1.8 s | B. | 等于1.2 s | C. | 大于1.8 s | D. | 小于1.8 s |
12.能正确表示下列反应的离子方程式是( )
| A. | 浓三氯化铁用于制作印刷线路板:Fe3++Cu═Fe2++Cu2+ | |
| B. | NaHSO4溶液中滴加Ba(OH)2溶液至中性:H++OH-+SO42-+Ba2+═BaSO4↓+H2O | |
| C. | NaHCO3溶液与NaAlO2溶液反应:HCO3-+AlO2-+H2O═Al(OH)3↓+CO2↑ | |
| D. | 向FeCl3溶液中加入Mg(OH)2:3Mg(OH)2+2Fe3+═2Fe(OH)3+3Mg2+ |
13.NA表示阿伏加德罗常数的值,下列说法正确的是( )
| A. | 0.1 mol甲烷含有的电子数为NA | |
| B. | 1 L 0.1 mol/L Na2CO3溶液中含有的CO32-数目为0.1 NA | |
| C. | 1 L pH=1的硫酸溶液中含有的H+数为0.2 NA | |
| D. | 1 mol•L-1 FeCl3溶液中所含Cl-的数目为3NA |
 .
. .
.