题目内容
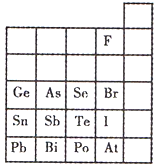 元素在周期表中的位置,反映了元素的原子结构和元素的性质.下图是元素周期表的一部分.
元素在周期表中的位置,反映了元素的原子结构和元素的性质.下图是元素周期表的一部分.(1)根据元素周期律预测:酸性强弱H3AsO4
<
<
H3PO4(用“>”或“<”表示).(2)元素Se的最高正价和最低负价的代数和为
4
4
;在一定条件下,S与H2反应有一定限度(可理解为反应进行的程度),请判断:在相同条件下Se与H2反应的限度比S与H2反应的限度小
小
(选填“大”、“小”或“相同”).(3)I2具有一定的氧化性,SO2具有较强的还原性,将适量SO2气体通入碘水后,溶液中主要存在的离子是
H+、I-、SO42-
H+、I-、SO42-
.(4)下列说法不正确的是
c
c
(填序号).a.C、N、O、F的原子半径随着原子序数的增大而减小
b.Si、P、S、Cl元素的非金属性随着核电荷数的增加而增强
c.干冰升华、水蒸气的液化都要吸热
d.HF、HCl、HBr、HI的热稳定性依次减弱.
分析:(1)同主族自上而下非金属性减弱,非金属性越强最高价含氧酸的酸性越强;
(2)Se处于ⅥA族,最高正化合价=族序数、最低负化合价=最外层电子数-8;
非金属性越弱,与氢气反应的限度越小;
(3)碘与二氧化硫、水反应生成硫酸与HI;
(4)a.同周期自左而右原子半径减小;
b.同周期自左而右非金属性增强;
c.水蒸气液化放出热量;
d.非金属性越强,氢化物越稳定.
(2)Se处于ⅥA族,最高正化合价=族序数、最低负化合价=最外层电子数-8;
非金属性越弱,与氢气反应的限度越小;
(3)碘与二氧化硫、水反应生成硫酸与HI;
(4)a.同周期自左而右原子半径减小;
b.同周期自左而右非金属性增强;
c.水蒸气液化放出热量;
d.非金属性越强,氢化物越稳定.
解答:解:(1)同主族自上而下非金属性减弱,非金属性P>As,非金属性越强最高价含氧酸的酸性越强,故酸性H3AsO4<H3PO4,
故答案为:<;
(2)Se处于ⅥA族,最高正化合价为+6,最低负化合价为-2,故元素Se的最高正价和最低负价的代数和为+6-2=4,Se与S处于同一主族,非金属性Se<S,Se与氢气反应的限度更小,
故答案为:4;小;
(3)发生反应I2+SO2+2H2O=4H++2I-+SO42-,故溶液中主要存在的离子是H+、I-、SO42-,
故答案为:H+、I-、SO42-;
(4)a.同周期自左而右原子半径减小,故C、N、O、F的原子半径随着原子序数的增大而减小,故a正确;
b.同周期自左而右非金属性增强,Si、P、S、Cl元素的非金属性随着核电荷数的增加而增强,故b正确;
c.冰液化吸收热量,水蒸气液化放出热量,故c错误;
d.非金属性F>Cl>Br>I,故HF、HCl、HBr、HI的热稳定性依次减弱,故d正确;
故答案为:c.
故答案为:<;
(2)Se处于ⅥA族,最高正化合价为+6,最低负化合价为-2,故元素Se的最高正价和最低负价的代数和为+6-2=4,Se与S处于同一主族,非金属性Se<S,Se与氢气反应的限度更小,
故答案为:4;小;
(3)发生反应I2+SO2+2H2O=4H++2I-+SO42-,故溶液中主要存在的离子是H+、I-、SO42-,
故答案为:H+、I-、SO42-;
(4)a.同周期自左而右原子半径减小,故C、N、O、F的原子半径随着原子序数的增大而减小,故a正确;
b.同周期自左而右非金属性增强,Si、P、S、Cl元素的非金属性随着核电荷数的增加而增强,故b正确;
c.冰液化吸收热量,水蒸气液化放出热量,故c错误;
d.非金属性F>Cl>Br>I,故HF、HCl、HBr、HI的热稳定性依次减弱,故d正确;
故答案为:c.
点评:本题考查元素周期表与元素周期律,难度不大,注意基础知识的理解掌握.

练习册系列答案
相关题目



