题目内容
15.(1)“服用维生素C,可使食物中的Fe3+还原成Fe2+”这句话说明,维生素C在这一反应中被氧化(氧化/还原),具有还原性,Fe3+发生了还原反应(氧化/还原).(2)市场上出售的某种麦片中含有微量的颗粒细小的还原性铁粉,这些铁粉在人体胃酸(主要成分是盐酸)的作用下转化成亚铁盐?此反应的化学方程式为Fe+2HCl=FeCl2+H2↑,离子方程式为Fe+2H+=Fe2++H2↑?
分析 (1)“服用维生素C,可使食物中的Fe3+还原成Fe2+”,Fe元素的化合价降低,则维生素C中某元素的化合价升高;
(2)铁粉在人体胃酸(主要成分是盐酸)的作用下转化成亚铁盐,Fe与盐酸反应生成氯化亚铁和氢气.
解答 解:(1)“服用维生素C,可使食物中的Fe3+还原成Fe2+”,Fe元素的化合价降低,则维生素C中某元素的化合价升高,则维生素C在这一反应中被氧化,具有还原性,Fe3+发生了还原反应,故答案为:氧化;还原;还原;
(2)铁粉在人体胃酸(主要成分是盐酸)的作用下转化成亚铁盐,Fe与盐酸反应生成氯化亚铁和氢气,化学反应为Fe+2HCl=FeCl2+H2↑,离子反应为Fe+2H+=Fe2++H2↑,故答案为:Fe+2HCl=FeCl2+H2↑.
点评 本题考查氧化还原反应,为高频考点,把握发生的反应及元素的化合价变化为解答的关键,侧重分析与应用能力的考查,题目难度不大.

练习册系列答案
 世纪百通期末金卷系列答案
世纪百通期末金卷系列答案
相关题目
6.Ca(OH)2溶解度随温度变化曲线如图所示,下列说法正确的是( )


| A. | 氢氧化钙的溶解是吸热过程 | |
| B. | 温度升高时氢氧化钙溶解的速度减慢 | |
| C. | t℃时氢氧化钙的 Ksp约等于2.46×10-6 | |
| D. | 向只含有Ca(OH)2 和Mg(OH)2]两种沉淀的悬浊液中滴加NaOH浓溶液,分散系中$\frac{c(C{a}^{2+})}{c(M{g}^{2+})}$比值不变 |
3.写出下列基团的名称:
| -C═C- | ─CH2CH3 或─C2H5 | ─OH | ─CHO | ─COOH | -COO-R |
10.下表所列各组物质中,物质之间通过一步反应就能实现如图所示转化的是( )
| 物质编号 | 物质转化关系 | 甲 | 乙 | 丙 | 丁 |
| ① | 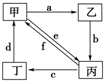 | Cu | CuO | CuCl2 | Cu(NO3)2 |
| ② | Na2CO3 | NaOH | NaHCO3 | CO2 | |
| ③ | (NH4)2SO3 | CaSO3 | SO2 | NH4HSO3 | |
| ④ | Al(OH)3 | Al2O3 | Na[Al(OH)4] | AlCl3 |
| A. | ①③ | B. | ②④ | C. | ②③④ | D. | ①②③④ |
7.下列有关物质结构的表述正确的是( )
| A. | 次氯酸的电子式 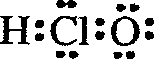 | B. | 二氧化硅分子式 SiO2 | ||
| C. | CS2结构式 S=C=S | D. | 钾离子的结构示意图如图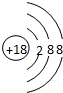 |
4.NA表示阿伏伽德罗常数,下列叙述正确的是( )
| A. | 1 mol FeI2与足量氯气反应时转移的电子数为2NA | |
| B. | 2 L 0.5 mol•L-1硫酸钾溶液中阴离子所带电荷数为NA | |
| C. | 1 mol Na2O2固体中含离子总数为4NA | |
| D. | 5NH4NO3$\frac{\underline{\;\;△\;\;}}{\;}$2HNO3+4N2↑+9H2O反应中,生成28 g N2时,转移的电子数目为3.75NA |
5.下列曲线示意图不正确的是( )
| A. | 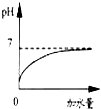 稀盐酸中滴加蒸馏水 | |
| B. | 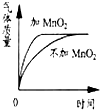 等体积、等质量分数的过氧化氢溶液分解 | |
| C. |  等质量、等颗粒大小的金属中加稀盐酸 | |
| D. |  HCl和FeCl3的混合溶液中滴加NaOH溶液 |

 ;水杨酸与小苏打溶液反应的化学方程式:
;水杨酸与小苏打溶液反应的化学方程式: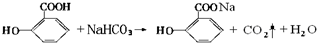 ;
;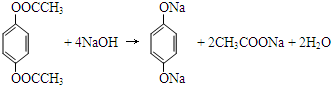 .
.