题目内容
下列电离方程式错误的是( )
| A.K2CO3═2K++CO32- | B.KClO3═K++Cl-+3O2- |
| C.NaOH═Na++OH- | D.NaHCO3═Na++HCO3- |
A、碳酸钾是溶于水的盐属于强电解质完全电离,电极方程式为K2CO3═2K++CO32-,故A正确;
B、氯酸钾是溶于水的盐属于强电解质,电离方程式为KClO3═K++ClO3-,故B错误;
C、氢氧化钠是溶于水的强碱完全电离,电离方程式为NaOH═Na++OH-,故C正确;
D、碳酸氢钠是弱酸强碱盐属于强电解质完全电离,电离方程式为NaHCO3═Na++HCO3-,故D正确;
故选B.
B、氯酸钾是溶于水的盐属于强电解质,电离方程式为KClO3═K++ClO3-,故B错误;
C、氢氧化钠是溶于水的强碱完全电离,电离方程式为NaOH═Na++OH-,故C正确;
D、碳酸氢钠是弱酸强碱盐属于强电解质完全电离,电离方程式为NaHCO3═Na++HCO3-,故D正确;
故选B.

练习册系列答案
相关题目

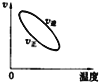


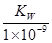 mol/L
mol/L CH3COO一+H+,对于该平衡,下列叙述不正确的是 ( )
CH3COO一+H+,对于该平衡,下列叙述不正确的是 ( )