��Ŀ����
����Ŀ���±���������ѧ��ѧ�̿�����Ԫ�����ڱ���һ���֣����е�ÿ����ű�ʾһ��Ԫ�أ������Ҫ��ش����⣺

��l���ڱ�ʾ��Ԫ���� ______ ����Ԫ�ط��ţ���
��2���ڢۢܢݢ�͢�������Ԫ�صļ����Ӱ뾶��С��������Ϊ��__________�������ӷ��ű�ʾ�����ϱ���ʾԪ���У��ǽ�������ǿ���� ______ ����Ԫ�ط��ţ����ߢ��������Ԫ�ص�����������Ӧ��ˮ�����������ǿ������˳��Ϊ��_______________�������ʽ��
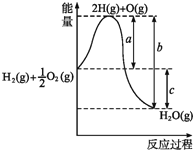
��3��Ԫ�آ�ĵ��ʿ���������ȡƯ�ۣ�Ư�۵���Ч�ɷ��� ______ ���ѧʽ�����õ���ʽ��ʾԪ�آ�����γɻ�����Ĺ��� ______ ��
��4������Ԫ���У���������ˮ���ҷ�Ӧ��ˮ����ԭ�����˵�����_________���ѧʽ��
��5��д��Ԫ�آܵ�����������Ӧ��ˮ������Ԫ�آ�������������Ӧ�Ļ�ѧ����ʽ ______ ��
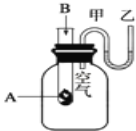
��6��ijͬѧΪ�˱Ƚ�Ԫ�آ�͢�ǽ����Ե����ǿ��������ͼ��ʾװ�ý���ʵ�飺
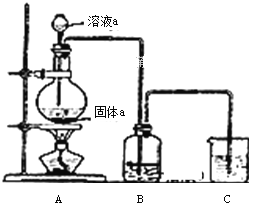
�� װ��B����Һ������Ϊ______��д��ѧʽ����
�� װ��C��ʢ���ռ�ϡ��Һ��Ŀ����______����Ӧ�����ӷ���ʽ��______
���𰸡� O Mg2+ < Na+ < F- < O2- < Cl- < S2- F HClO4 > H2SO4 > H3PO4 Ca��ClO��2 ![]() F2 Al2O3 + 2 NaOH = 2 NaAlO2 + H2O Na2S����H2S�� ���ն����Cl2 Cl2 + 2OH- = Cl- + ClO- + H2O
F2 Al2O3 + 2 NaOH = 2 NaAlO2 + H2O Na2S����H2S�� ���ն����Cl2 Cl2 + 2OH- = Cl- + ClO- + H2O
������������Ԫ�������ڱ��е����λ�ÿ�֪�١���ֱ���N��O��F��Na��Mg��Al��P��S��Cl����
��l���ڱ�ʾ��Ԫ����O����2�����ӵĺ�����Ӳ���Խ�࣬���Ӱ뾶Խ��������Ų���ͬʱ���Ӱ뾶��ԭ���������������С����ڢۢܢݢ�͢�������Ԫ�صļ����Ӱ뾶��С��������ΪMg2+��Na+��F- ��O2-��Cl-��S2-���ϱ���ʾԪ���У��ǽ�������ǿ����F���ǽ�����Խǿ����ۺ����������Խǿ���ߢ��������Ԫ�ص�����������Ӧ��ˮ�����������ǿ������˳��ΪHClO4��H2SO4��H3PO4����3��Ư�۵���Ч�ɷ���Ca��ClO��2��Ԫ�آ�����γɻ��������Ȼ�þ�����γɹ��̿ɱ�ʾΪ ����4������Ԫ���У���������ˮ���ҷ�Ӧ��ˮ����ԭ����F2����5��Ԫ�آܵ�����������Ӧ��ˮ������Ԫ�آ�������������Ӧ�Ļ�ѧ����ʽΪAl2O3+2NaOH��2NaAlO2+H2O����6����Ҫ��֤��Ԫ�صķǽ�����ǿ��������������������û���Ӧ�жϣ���װ��B����Һ������ΪNa2S��H2S����װ��C��ʢ���ռ�ϡ��Һ��Ŀ�������ն����Cl2����ֹ��Ⱦ��������Ӧ�����ӷ���ʽ��Cl2+2OH-��Cl-+ClO- +H2O��
����4������Ԫ���У���������ˮ���ҷ�Ӧ��ˮ����ԭ����F2����5��Ԫ�آܵ�����������Ӧ��ˮ������Ԫ�آ�������������Ӧ�Ļ�ѧ����ʽΪAl2O3+2NaOH��2NaAlO2+H2O����6����Ҫ��֤��Ԫ�صķǽ�����ǿ��������������������û���Ӧ�жϣ���װ��B����Һ������ΪNa2S��H2S����װ��C��ʢ���ռ�ϡ��Һ��Ŀ�������ն����Cl2����ֹ��Ⱦ��������Ӧ�����ӷ���ʽ��Cl2+2OH-��Cl-+ClO- +H2O��

 �ܿ�����ĩ��̾�ϵ�д�
�ܿ�����ĩ��̾�ϵ�д�����Ŀ��ijʵ��С����������KMnO4��H2C2O4��Ӧͨ���ⶨ��λʱ�������� CO2������̽��Ӱ�췴Ӧ���ʵ����أ����ʵ�鷽�������
ʵ����� | A ��Һ | B ��Һ |
�� | 20 mL 0.1 molL��1 H2C2O4 ��Һ | 30 mL 0.01 molL��1KMnO4 ������Һ |
�� | 20 mL 0.2 molL��1 H2C2O4 ��Һ | 30 mL 0.01 molL��1 KMnO4������Һ |

��1��������ͼװ�������Ե����㷽��Ϊ�� ��
��2��H2C2O��Һ������ KMnO4��Һ��Ӧ�Ļ�ѧ����ʽΪ ��
��3����ʵ��̽���������ضԻ�ѧ��Ӧ���ʵ�Ӱ�죬��ͬʱ������Ͳ������CO2�������С��ϵ������ʵ����ţ���
��4����ʵ�����2minĩ�ռ���4.48mL CO2����״���£�������2minĩ��c��MnO4����=����������Һ���ǰ������ı仯����
��5��С��ͬѧ���ַ�Ӧ����������ͼ��ʾ������̽��t1��t2ʱ�������ʱ�����Ҫԭ�������������ǣ�����������K+�Ը÷�Ӧ�д����ã�