题目内容
【题目】(1)标准状况下,1.92g某气体的体积为672mL,则该气体的摩尔质量为_____;
(2)9.5克某金属氯化物MCl2 中含有0.200molCl-,则该氯化物的摩尔质量为 ______________,金属M的相对原子质量为 ______________。
(3)同温同压时,某气体A对氢气的相对密度为22。则在标准状况下,气体A的密度为________g/L ,质量为4.4g的气体A所含有的分子数约为__________。
【答案】64g/mol 95g/mol 24 1.96 6.02x1022。
【解析】
(1)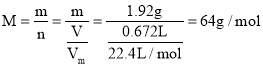 ;
;
(2)1molMCl2中含2mol氯离子,故含有0.200molCl-时,MCl2的物质的量为0.1mol,其摩尔质量![]() ,金属M的相对原子质量为95-71=24;
,金属M的相对原子质量为95-71=24;
(3)同温同压时,某气体A对氢气的相对密度为22,则该气体的摩尔质量为44g/mol,标准状况下,气体A的密度为![]() ,质量为4.4g的气体A的物质的量为0.1mol,故分子数为6.02×1022。
,质量为4.4g的气体A的物质的量为0.1mol,故分子数为6.02×1022。

练习册系列答案
 口算心算速算应用题系列答案
口算心算速算应用题系列答案 同步拓展阅读系列答案
同步拓展阅读系列答案
相关题目






