题目内容
【题目】判断含氧酸强弱的一条经验规律:含氧酸分子结构中含非羟基氧原子数越多,该含氧酸的酸性越强。几种实例如下表所示。

(1)亚磷酸(H3PO3)和亚砷酸(H3AsO3)的分子式相似,但它们的酸性差别很大。亚磷酸是中强酸,亚砷酸既有弱酸性又有弱碱性,由此可推出它们的结构式分别为:亚磷酸_________,亚砷酸________。
(2)亚磷酸和亚砷酸与过量的NaOH溶液反应的化学方程式分别是:亚磷酸:_____,亚砷酸:______。
(3)在亚磷酸和亚砷酸中分别加入浓盐酸,分析反应情况,写出化学方程式________________。
【答案】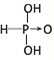
![]() H3PO3+2NaOH=Na2HPO3+2H2O H3AsO3+3NaOH=Na3AsO3+3H2O 亚磷酸是中强酸和盐酸不反应,亚砷酸和盐酸能反应,反应方程式为As(OH)3+3HCl=AsCl3+3H2O
H3PO3+2NaOH=Na2HPO3+2H2O H3AsO3+3NaOH=Na3AsO3+3H2O 亚磷酸是中强酸和盐酸不反应,亚砷酸和盐酸能反应,反应方程式为As(OH)3+3HCl=AsCl3+3H2O
【解析】
(1)含氧酸分子结构中含非羟基氧原子数越多,该含氧酸的酸性越强,据此确定酸的结构式;
(2)酸和碱反应生成盐和水,亚磷酸中含有2个羟基,属于二元酸,亚砷酸属于三元酸。
(3) 亚磷酸为中强酸,不与盐酸反应,亚砷酸为两性物质,可与盐酸反应。
(1)含氧酸分子结构中含非羟基氧原子数越多,该含氧酸的酸性越强,亚磷酸是中强酸,亚砷酸既有弱酸性又有弱碱性,所以亚磷酸和亚砷酸的结构式分别为: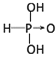 、
、![]() ,
,
综上所述,本题答案是: 、
、![]() 。
。
(2)酸和碱反应生成盐和水,亚磷酸中含有2个羟基,属于二元酸,亚砷酸属于三元酸,亚磷酸和氢氧化钠反应生成Na2HPO3,反应方程式为:H3PO3+2NaOH=Na2HPO3+2H2O;亚砷酸和氢氧化钠反应生成Na3AsO3,反应方程式为:H3AsO3+3NaOH=Na3AsO3+3H2O;
综上所述,本题答案为:H3PO3+2NaOH=Na2HPO3+2H2O、H3AsO3+3NaOH=Na3AsO3+3H2O。
(3) 亚磷酸为中强酸,不与盐酸反应,亚砷酸为两性物质,可与盐酸反应生成AsCl3和H2O,反应方程式为As(OH)3+3HCl=AsCl3+3H2O;
综上所述,本题答案是:亚磷酸是中强酸和盐酸不反应,亚砷酸和盐酸能反应,As(OH)3+3HCl=AsCl3+3H2O。

【题目】下列实验操作、现象和结论均正确的是
选项 | 实验操作 | 现象 | 结论 |
A | 等体积pH=2的HX和HY两种酸分别与足量的铁反应,用排水法收集气体 | HX放出的氢气多且反应速率快 | 酸的强弱:HX<HY |
B | 向2 mL 0.1 mol/L Na2S溶液中滴2滴0.1 mol/L ZnSO4溶液;再滴2滴0.1 mol/L CuSO4 | 先生成白色沉淀,后生成黑色沉淀 | 溶度积(Ksp):ZnS>CuS |
C | 向FeCl3和KSCN混合溶液中,加入少量KCl的固体 | 溶液颜色变浅 | FeCl3+3KSCN |
D | 常温下,用pH计分别测定饱和NaA溶液和饱和NaB溶液的pH | pH:NaA>NaB | 常温下酸性:HA﹤HB |
A. A B. B C. C D. D
【题目】实验室模拟侯氏制碱法原理,可以制备一些常见的化合物。
i. 30℃时,向饱和NaCl溶液中加入NH4HCO3细粉,制备NaHCO3晶体。
(1)已知30℃时几种盐的溶解度为:
物质 | NaCl | NH4HCO3 | NaHCO3 | NH4Cl |
S(g/100gH2O) | 36.3 | 27.0 | 11.1 | 41.1 |
书写化学方程式_______________________。根据反应原理结合信息解释NaHCO3易析出的原因__________________________。

(2)过滤出NaHCO3晶体后,为继续分离滤液中的物质,设计如图装置。左侧发生装置可制取氨气,原因是_____________。一段时间后,试管中析出白色晶体为_______。用冰水浴降温目的是_____________。
ii. 制取(NH4)2SO4晶体的流程如下:

(3)“转化”步骤中CO2不宜过量,原因是__________________。
(4)操作I和II所需的实验步骤顺序是____________(选填编号,可重复选择)。
a. 蒸发浓缩 b. 蒸馏 c. 过滤 d. 萃取 e. 分液 f. 冷却结晶
(5)为测定某硫酸铵样品(杂质为碳酸铵)纯度。先准确称取5.000g样品溶于水,加入足量的_______,再加入足量BaCl2溶液充分反应后过滤、洗涤沉淀并烘干至恒重,最终所得固体为8.155g。则硫酸铵样品的纯度为___________。



