题目内容
【题目】下列关于反应过程中能量变化的说法正确的是
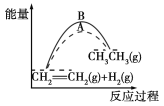
A.在一定条件下,某可逆反应的ΔH=+100 kJ·mol-1,则该反应的正反应活化能比逆反应活化能大100 kJ·mol-1
B.图中A、B曲线可分别表示反应CH2=CH2(g)+H2(g)=== CH3CH3(g)未使用催化剂和使用催化剂时反应过程中的能量变化
C.同温同压下,反应H2(g)+Cl2(g)===2HCl(g)在光照和点燃条件下的ΔH不同
D.由如图所示的能量变化可判断出该化学反应是放热反应
【答案】A
【解析】A项,可逆反应的正、逆反应的活化能之差等于该反应的反应热,A项正确。B项,催化剂降低反应所需的活化能,即A曲线表示的过程使用了催化剂,B项错误。C项,同一化学反应的ΔH相同,C项错误。D项,图示反应为吸热反应,D项错误。

【题目】已知某反应的平衡常数表达式为:K=![]() 其平衡常数随温度变化如下表所示:请回答下列问题:
其平衡常数随温度变化如下表所示:请回答下列问题:
温度/℃ | 400 | 500 | 850 |
平衡常数 | 9.94 | 9 | K1 |
(1)该反应的ΔH______0(填“>”或“<”)。
(2)若在500 ℃时进行上述反应,某时刻测得四种物质的体积分数彼此相等,则此时反应_____向进行中(“正”或“逆”);
(3)850 ℃时在一个固定体(反应器中,投入2 molCO和3 molH2O(g),发生上述反应,CO和H2O(g)的浓度变化如图所示,则
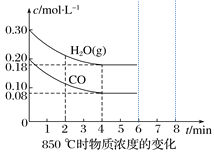
①4 min时H2的物质的量分数=___________;②K1=_____________;
③若4分钟时测得反应的热效应数值为a kJ,则该反应的热化学方程式为:_________;
④若第6分钟将容器压缩为5L,画出6~8分钟CO的浓度变化图像(注明起点坐标)______________;
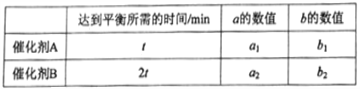
(4)t1℃(高于850℃)时,在相同容器中发生上述反应,容器内各物质的浓度随时间变化如下表。
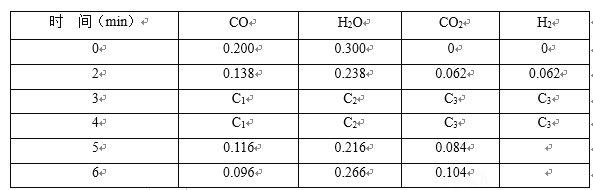
①3~4min时,v正________v逆(填“>”或“=”或“<”),C1 ____0.08 mol/L(填“>”或“=”或“<”);
②反应在4 min~5 min,平衡向逆方向移动,可能的原因是_________ (单选),反应在5 min~6 min,平衡向正方向移动,可能的原因是___________ (单选)。
A.增加水蒸气 B.降低温度 C.使用催化剂 D.增加氢气浓度