题目内容
10.下列各组混合物中,用分液漏斗不能分离的是( )| A. | 植物油和水 | B. | 乙酸乙酯和水 | C. | 四氯化碳和苯 | D. | 苯和水 |
分析 根据分液漏斗可以将互不相溶的两层液体分开,则分析选项中物质的溶解性即可.
解答 解:A.植物油和水不溶,能用分液漏斗进行分离,故A错误;
B.乙酸乙酯和水不溶,能用分液漏斗进行分离,故B错误;
C.四氯化碳和苯互溶,不能用分液漏斗进行分离,故C正确;
D.苯和水不溶,能用分液漏斗进行分离,故D错误;
故选C.
点评 本题考查了物质的分离和提纯,难度不大,注意分液漏斗能分离的物质必须是互不相溶的液体.

练习册系列答案
 天天向上一本好卷系列答案
天天向上一本好卷系列答案 小学生10分钟应用题系列答案
小学生10分钟应用题系列答案
相关题目
20.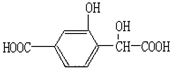 某有机物的结构简式如图所示,1mol的该有机物分别和足量的Na、NaOH、NaHCO3反应时,消耗三种物质的物质的量之比是( )
某有机物的结构简式如图所示,1mol的该有机物分别和足量的Na、NaOH、NaHCO3反应时,消耗三种物质的物质的量之比是( )
 某有机物的结构简式如图所示,1mol的该有机物分别和足量的Na、NaOH、NaHCO3反应时,消耗三种物质的物质的量之比是( )
某有机物的结构简式如图所示,1mol的该有机物分别和足量的Na、NaOH、NaHCO3反应时,消耗三种物质的物质的量之比是( )| A. | 1:1:1 | B. | 1:1:2 | C. | 4:3:2 | D. | 2:3:2 |
1.室温下,对于0.10mol•L-1的氨水,下列判断正确的是( )
| A. | 其溶液中的c(OH-)═0.1mol•L-1 | |
| B. | k加水稀释后,溶液中c(NH4+)•c(OH-)变大 | |
| C. | 加水稀释后,水电离出的c(H+)变大 | |
| D. | 与AlCl3溶液发生反应的离子方程式为:Al3++3OH-═Al(OH)3↓ |
18.下列叙述错误的是( )
| A. | 油脂、淀粉、糖类和蛋白质在一定条件都能发生水解反应 | |
| B. | 向鸡蛋清的溶液中滴加饱和Na2SO4溶液,有固体析出,若加入足量蒸馏水,固体会重新溶解 | |
| C. | 将红热的铜丝迅速插入乙醇中,可观察到铜丝表面变红,并能闻到刺激性气味 | |
| D. | 煤干馏后可以得到煤焦油 |
5.一定条件下存在反应:H2(g)+I2(g)?2HI(g)△H<0,现有三个相同的1L恒容绝热(与外界没有热量交换)密闭容器Ⅰ、Ⅱ、Ⅲ,按下列配比充入气体,700℃条件下开始反应,达到平衡时,下列说法正确的是( )
①在Ⅰ中充入1mol H2和1mol I2(g)
②在Ⅱ中充入2mol HI(g)
③在Ⅲ中充入2mol H2和2mol I2(g)
①在Ⅰ中充入1mol H2和1mol I2(g)
②在Ⅱ中充入2mol HI(g)
③在Ⅲ中充入2mol H2和2mol I2(g)
| A. | 容器Ⅰ、Ⅱ中正反应速率相同 | |
| B. | 容器Ⅰ、Ⅲ中反应的平衡常数相同 | |
| C. | 容器Ⅰ中的气体颜色比容器Ⅱ中的气体颜色深 | |
| D. | 容器Ⅰ中H2的转化率与容器Ⅱ中HI的转化率之和等于1 |
15.下列有机物不能互称为同分异构体的是( )
| A. | 丙酸和乙酸甲酯 | B. | 淀粉和纤维素 | C. | 葡萄糖和果糖 | D. | 蔗糖和麦芽糖 |
2.下列实验中,分离提纯的方法不正确的是( )
| 选项 | 实验 | 分离、提纯方法 |
| A | 提纯粗苯甲酸 | 重结晶 |
| B | 分离乙醇和丁醇 | 蒸馏 |
| C | 除去乙炔中的H2S气体 | 用CuSO4溶液洗气 |
| D | 除去苯中的苯酚 | 加入NaOH溶液后过滤 |
| A. | A | B. | B | C. | C | D. | D |
5.硼酸(H3BO3)大量应用于玻璃制造行业,以硼镁矿(2MgO•B2O3•H2O、SiO2及少量Fe3O4、CaCO3,Al2O3)为原料生产硼酸的工艺流程如图1:

已知:H3BO3在20℃、40℃、60℃、100℃时的溶解度依次为5.0g、8.7g、14.8g、40.2g.Fe3+、Al3 +、Fe2+和Mg2 +以氢氧化物形式完全沉淀时,溶液的pH分别为3.2、5.2、9.7和 12.4.
(1)由于矿粉中含CaCO3,为防止“浸取”时容易产生大量泡沫使物料从反应器中溢出,应采取的措施是:分批慢慢加入稀硫酸.
(2)“浸出液”显酸性,含H3BO3和Mg2+和SO42-,还含有Fe2+、Fe3+、Ca2+、Al3+等杂质.“除杂”时向浸出液中依次加入适量H2O2和MgO,除去的杂质离子是Fe3+、Fe2+、Al3+.H2O2的作用是H2O2+2H++2Fe2+=2Fe3++2H2O (用离子方程式表示).
(3)“浸取”后,采用“热过滤”的目的是防止温度下降时H3BO3从溶液中析出.
(4)“母液”可用于回收硫酸镁,已知硫酸镁的溶解度随温度变化的曲线如图2,且溶液的沸点随压强增大而升高.为了从“母液”中充分回收MgSO4•H20,应采取的 措施是将“母液”蒸发浓缩,加压升温结晶
(5)已知298K时,硼酸(H3BO3)溶液中存在如下反应:H3BO3(aq)+H2O(l)?[B(OH)4]-(aq)+H+(aq) K=5.7×10-10
下列说法正确的是BD.
A.碳酸钠溶液滴入硼酸中能观察到有气泡产生
B.碳酸钠溶液滴入醋酸中能观察到有气泡产生
C.等浓度的碳酸和硼酸溶液比较,pH:前者>后者
D.等浓度的碳酸钠和醋酸钠溶液比较,pH:前者>后者.

已知:H3BO3在20℃、40℃、60℃、100℃时的溶解度依次为5.0g、8.7g、14.8g、40.2g.Fe3+、Al3 +、Fe2+和Mg2 +以氢氧化物形式完全沉淀时,溶液的pH分别为3.2、5.2、9.7和 12.4.
(1)由于矿粉中含CaCO3,为防止“浸取”时容易产生大量泡沫使物料从反应器中溢出,应采取的措施是:分批慢慢加入稀硫酸.
(2)“浸出液”显酸性,含H3BO3和Mg2+和SO42-,还含有Fe2+、Fe3+、Ca2+、Al3+等杂质.“除杂”时向浸出液中依次加入适量H2O2和MgO,除去的杂质离子是Fe3+、Fe2+、Al3+.H2O2的作用是H2O2+2H++2Fe2+=2Fe3++2H2O (用离子方程式表示).
(3)“浸取”后,采用“热过滤”的目的是防止温度下降时H3BO3从溶液中析出.
(4)“母液”可用于回收硫酸镁,已知硫酸镁的溶解度随温度变化的曲线如图2,且溶液的沸点随压强增大而升高.为了从“母液”中充分回收MgSO4•H20,应采取的 措施是将“母液”蒸发浓缩,加压升温结晶
(5)已知298K时,硼酸(H3BO3)溶液中存在如下反应:H3BO3(aq)+H2O(l)?[B(OH)4]-(aq)+H+(aq) K=5.7×10-10
| 化学式 | 碳酸 | 醋酸 |
| 电离常数 | K1=4.4×10-7K2=4.7×10-11 | K=1.75×10-5 |
A.碳酸钠溶液滴入硼酸中能观察到有气泡产生
B.碳酸钠溶液滴入醋酸中能观察到有气泡产生
C.等浓度的碳酸和硼酸溶液比较,pH:前者>后者
D.等浓度的碳酸钠和醋酸钠溶液比较,pH:前者>后者.