题目内容
【题目】下列离子方程式书写正确的是
A. 铁和盐酸溶液反应:2Fe + 6H+ === 2Fe3+ +3 H2↑
B. 氯气和水反应:Cl2 + H2O![]() 2 H+ + Cl- + ClO
2 H+ + Cl- + ClO
C. 氢氧化钡溶液与硫酸铜溶液反应:Ba2+ + SO42- = BaSO4↓
D. 氯化铁溶液与氨水溶液反应: Fe3+ + 3 NH3·H2O === Fe (OH)3 ↓+ 3NH4+
【答案】D
【解析】
A.铁和盐酸溶液反应生成Fe2+ 和 H2,故A错误;B.氯气和水反应生成的HClO是弱酸,不可折,故B错误;C.氢氧化钡溶液与硫酸铜溶液反应生成BaSO4和Cu(OH)2沉淀,故C错误;D.氯化铁溶液中滴加氨水溶液发生反应的离子方程式为Fe3+ + 3 NH3·H2O === Fe (OH)3 ↓+ 3NH4+,故D错误;答案为D。

练习册系列答案
相关题目
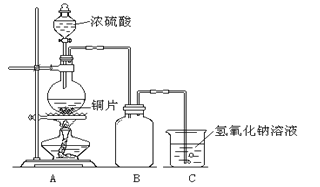
【题目】实验室中某些气体的制取、收集及尾气处理装置如图所示(省略夹持和净化装置)。仅用此装置和表中提供的物质完成相关实验,最合理的选项是

选项 | a中的物质 | b中的物质 | c中收集的气体 | d中的物质 |
A | 浓氨水 | CaO | NH3 | H2O |
B | 浓硫酸 | Na2SO3 | SO2 | NaOH溶液 |
C | 稀硝酸 | Cu | NO2 | H2O |
D | 浓盐酸 | MnO2 | Cl2 | NaOH溶液 |
A. A B. B C. C D. D