题目内容
【题目】下图为足量铜与浓硫酸反应的装置。请回答:
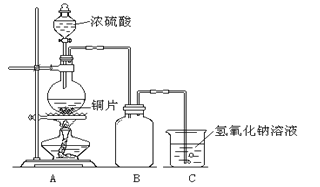
(1)写出盛放有铜片的仪器名称____________。
(2)检查装置气密性的操作为____________。
(3)下列有关该实验的说法中正确的是____________。
A.烧杯中氢氧化钠溶液的作用是吸收尾气,防止空气污染
B.实验时可以观察到圆底烧瓶中溶液由无色最终变为蓝色
C.含 0.08 mol 溶质的浓硫酸与足量的铜片反应,能收集到896mL(标准状况)的SO2
D.在该实验中浓硫酸体现了酸性和强氧化性
E.如果 B 中盛有少量 KMnO4 溶液,反应一段时间后,可以观察到紫色褪去,说明SO2具有漂白性。
【答案】圆底烧瓶连接好装置,关闭分液漏斗旋塞,将导管末端插入水中,给圆底烧瓶微热(或用手掌紧捂圆底烧瓶外壁),如果导管口产生气泡,停止微热后(或移开手掌后)导管内形成一段稳定的水柱,说明气密性良好AD
【解析】
(1)铜片盛放在圆底烧瓶中在加热条件下与浓硫酸反应;
(2)连接好该装置,关闭分液漏斗旋塞,将导管末端插入水中,给圆底烧瓶微热(或用手掌紧捂圆底烧瓶外壁),如果导管口产生气泡,停止微热后(或移开手掌后)导管内形成一段稳定的水柱,说明气密性良好
(3)A.尾气SO2有毒,对环境有污染,但能溶解于NaOH溶液,可利用氢氧化钠溶液吸收其尾气,防止空气污染,故A正确;B.因选用的是浓硫酸,生成的CuSO4以固体形式析出在烧杯底部,无法观察到圆底烧瓶中溶液由无色最终变为蓝色,故B错误;C.随反应的进行,当硫酸浓度降低后,铜和稀硫酸不再反应,故C错误;D.在铜和浓硫酸的反应中,体现了浓硫酸的酸性和强氧化性,故D正确;E.SO2具有还原性,能使酸性 KMnO4 溶液紫色褪去,故E错误;答案为AD。

练习册系列答案
 开心快乐假期作业暑假作业西安出版社系列答案
开心快乐假期作业暑假作业西安出版社系列答案 名题训练系列答案
名题训练系列答案 期末集结号系列答案
期末集结号系列答案
相关题目