题目内容
【题目】某化学实验小组同学利用以下装置制备氨气,并探究氨气的性质(部分仪器已略去)。

请回答:
(1)该同学用镊子夹取湿润的红色石蕊试纸靠近试管口,可观察到试纸变蓝,该现象说明氨气溶于水,溶液呈___性。
(2)收集氨气时,请你选择氨气的进气口___(“a”或“b”)。
(3)若观察到装置B中的烧瓶内产生了红色喷泉,则说明氨气具有的性质是___。
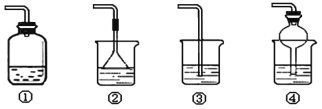
(4)以下装置(盛放的液体均为水)可用于吸收多余氨气的是___(填序号)。
【答案】碱 a 极易溶于水,且与水反应生成一种碱性物质 ②④
【解析】
(1)利用氨气溶于水生成NH3·H2O进行分析;
(2)氨气的密度小于空气,收集时用向下排空气法收集,对此进行分析;
(3)根据(1)的分析;
(4)氨气极易溶于水,吸收时注意防倒吸;
(1)NH3极易溶于水,在水中有NH3++H2O![]() NH3·H2O
NH3·H2O![]() NH4++OH-,酚酞遇碱变蓝,因此该实验体现了溶液呈碱性;
NH4++OH-,酚酞遇碱变蓝,因此该实验体现了溶液呈碱性;
(2)氨气的密度小于空气的密度,收集时应向下排空气法收集,即从a口进气;
(3) 形成喷泉,说明烧瓶的压强突然减小,即推出NH3极易溶于水,酚酞遇碱变蓝,说明氨气溶于水后,生成一种碱性物质;
(4)氨气极易溶于水,可以用水吸收多余的氨气,吸收时应注意防治倒吸,故②④正确。

 步步高口算题卡系列答案
步步高口算题卡系列答案 点睛新教材全能解读系列答案
点睛新教材全能解读系列答案 小学教材完全解读系列答案
小学教材完全解读系列答案【题目】已知反应A(g)+B(g) ![]() C(g)+D(g)的平衡常数K值与温度的关系如表所示,830 ℃时,向一个2 L的密闭容器中充入0.20 mol A和0.20 mol B,10 s时达平衡。下列说法不正确的是
C(g)+D(g)的平衡常数K值与温度的关系如表所示,830 ℃时,向一个2 L的密闭容器中充入0.20 mol A和0.20 mol B,10 s时达平衡。下列说法不正确的是
温度/℃ | 700 | 830 | 1200 |
K值 | 1.7 | 1.0 | 0.4 |
A. 达到平衡后,B的转化率为50%
B. 增大压强,正、逆反应速率均加快
C. 该反应为吸热反应,升高温度,平衡正向移动
D. 反应初始至平衡,A的平均反应速率v(A)=0.005 mol·L-1·s-1