题目内容
【题目】下表为元素周期表的一部分,参照元素①~⑦在表中的位置,请用化学用语回答下列问题:
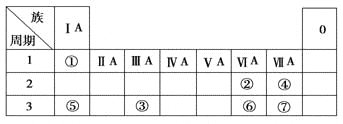
(1)③⑤⑥⑦中原子半径最大的是 (用元素符号表示,下同),②③④⑤的简单离子中半径最小的是 。
(2)③⑤中元素的金属性强弱顺序为 ,⑥⑦元素的非金属性强弱顺序为 。
(3)①、②两种元素按原子个数比为1∶1组成的常见液态化合物,在酸性溶液中能将Fe2+氧化,写出该反应的离子方程式 。
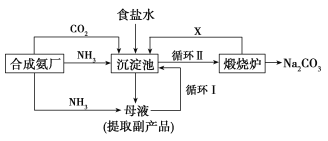
(4)由表中元素形成的物质可发生如图中的反应,其中B、C、G是单质,B为黄绿色气体,D溶液显碱性。

①写出D溶液与G反应的化学方程式 。
②写出电解A溶液的化学方程式: 。
③若上图中E、F按等物质的量进行反应,则混合物X中含有的物质有 (水忽略) 。
【答案】(1)Na Al3+
(2) Na>Al、Cl>S
(3)H2O2+2Fe2++2H+=2Fe3++2H2O
(4)①2Al+2NaOH+2H2O=2NaAlO2+3H2↑;②2NaCl+2H2O![]() 2NaOH+H2↑+Cl2↑;③Al(OH)3、NaCl
2NaOH+H2↑+Cl2↑;③Al(OH)3、NaCl
【解析】试题分析:由元素子周期表中位置可知①为H、②为O、③为Al、④为F、⑤为Na、⑥为S、⑦为Cl。
(1)自左而右原子半径减小,同主族自上而下原子半径增大,因此原子半径最大的是Na;离子的核外电子层数越多,离子半径越大,核外电子排布相同时离子半径越小,则②③④⑤的简单离子中半径最小的是Al3+;
(2)同周期自左向右金属性逐渐减弱,则③⑤中元素的金属性强弱顺序为Na>Al;同周期自左向右非金属性逐渐增强,则⑥⑦元素的非金属性强弱顺序为Cl>S;
(3)①、②两种元素按原子个数之比为1:1组成的常见液态化合物为H2O2,在酸性溶液中能将Fe2+氧化Fe3+,同时生成水,反应离子方程式为H2O2+2Fe2++2H+=2Fe3++2H2O;
(4)由表中元素形成的物质,其中B、C、G是单质,B为黄绿色气体,则B为Cl2,D溶液显碱性,电解A溶液为电解氯化钠溶液生成氢气、氯气与氢氧化钠,故D为NaOH、C为H2、E为HCl,G能与氢氧化钠溶液反应得到得到氢气,故G为Al,F为NaAlO2;
①D溶液与G反应的化学方程式为2Al+2NaOH+2H2O=2NaAlO2+3H2↑;
②电解氯化钠溶液的化学方程式为2NaCl+2H2O![]() 2NaOH+H2↑+Cl2↑;
2NaOH+H2↑+Cl2↑;
③盐酸和偏铝酸钠按等物质的量进行反应,恰好反应生成氢氧化铝和氯化钠,即混合物X中含有的物质有Al(OH)3、NaCl。