题目内容
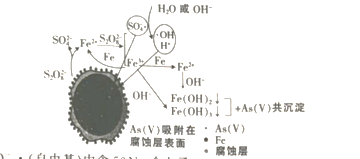
【题目】某兴趣小组设计如下微型实验装置。实验时,发现断开K2,闭合K1,两极均有气泡产生;一段时间后,断开K1,闭合K2,发现电流表指针偏转,下列有关描述正确的是
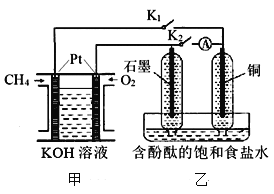
A. 断开K2,闭合K1时,石墨电极上的电极反应式为:2 H++ 2e-=H2↑
B. 断开K1,闭合K2时,铜电极上的电极反应式为:Cl2 + 2e-=2Cl-
C. 甲装置属于燃料电池,该电池正极的电极反应式为:CH4+10OH--8e-=CO32-+7H2O
D. 甲烷燃料电池的总电极反应式为:CH4+2O2 +2NaOH=Na2CO3+3H2O
【答案】D
【解析】
实验时,断开K2,闭合K1,乙装置是电解池,石墨作阳极,铜是阴极,阳极上氯离子放电生成氯气,阴极上氢离子放电生成氢气,所以两极均有气泡产生;一段时间后,断开K1,闭合K2,乙池形成氢氯燃料电池,铜作负极氢气失电子发生氧化反应,石墨作正极,氯气得电子发生还原反应。
实验时,断开K2,闭合K1,乙装置是电解池,石墨作阳极,铜是阴极,阳极上氯离子放电生成氯气,阴极上氢离子放电生成氢气,所以两极均有气泡产生;一段时间后,断开K1,闭合K2,乙池形成氢氯燃料电池,铜作负极氢气失电子发生氧化反应,石墨作正极,氯气得电子发生还原反应;
A.断开K2,闭合K1时,该装置是电解池,铜作阴极,石墨作阳极,石墨电极上氯离子失电子发生氧化反应,所以其电极反应式为:2Cl--2e-=Cl2↑,故A错误;
B.断开K1,闭合K2时,该装置是原电池,铜作负极,负极上氢气失电子发生氧化反应,所以铜电极上的电极反应式为:H2-2e-═2H+,故B错误;
C.甲装置属于燃料电池,该电池正极上氧气得电子发生还原反应,该电池正极的电极反应式为O2十2H2O+4e-=4OH-,故C错误;
D.甲装置属于燃料电池,甲烷和氧气、氢氧化钠反应生成碳酸钠和水,所以总电极反应式为:CH4+2O2+2NaOH=Na2CO3+3H2O,故D正确;
故答案为D。

 七星图书口算速算天天练系列答案
七星图书口算速算天天练系列答案 初中学业考试导与练系列答案
初中学业考试导与练系列答案【题目】硫酸铜晶体(CuSO4·![]() H2O蓝色)在110℃开始失去结晶水,150℃失去全部结晶水,生成白色的无水硫酸铜。依据硫酸铜晶体受热失去结晶水的事实,可以设计硫酸铜晶体水含量
H2O蓝色)在110℃开始失去结晶水,150℃失去全部结晶水,生成白色的无水硫酸铜。依据硫酸铜晶体受热失去结晶水的事实,可以设计硫酸铜晶体水含量![]() 的测定方法。请根据以下实验数据回答相关问题:(M(CuSO4)=159.5g/mol、M(H2O)=18.0g/mol)
的测定方法。请根据以下实验数据回答相关问题:(M(CuSO4)=159.5g/mol、M(H2O)=18.0g/mol)
坩埚质量 | 坩埚和晶体的质量 | 完全失去结晶水后坩埚和剩余固体的质量 |
11.685g | 13.691g | 12.948g |
(1)要完成此实验,至少要称量______次。
(2)![]() ______(保留2位小数),本次实验结果____(填“偏高”、“偏低”)。
______(保留2位小数),本次实验结果____(填“偏高”、“偏低”)。
(3)造成本次误差可能的原因是______。
A. 加热时有晶体溅出
B. 实验前坩埚内有受热不挥发、不分解也不与硫酸铜反应的杂质
C. 粉末未完全变白就停止加热
D. 加热后放在空气中冷却
(4)请写出造成本次误差还有可能存在的其他原因(写出其中一点)_____________________。
(5)如果硫酸铜晶体样品不纯,测定结果________。
A.没有偏差 B. 一定偏小 C. 一定偏大 D. 无法确定