题目内容
【题目】由A、B、C、D四种金属按下表中装置进行实验,根据实验现象填表:
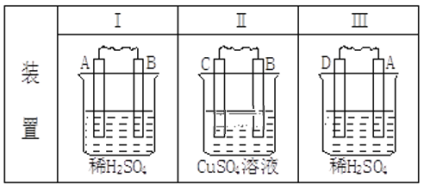
现象 | (I)金属A逐渐溶解 | (Ⅱ)C的质量增加 | (Ⅲ)A上有气体产生 |
填正极反应式 | ___ | ___ | |
四种金属活动性由强到弱的顺序:___。 | |||
若装置(Ⅲ)中A极产生的气体在标准状况下的体积为224mL,则通过导线中的电子的物质的量为___mol。 | |||
【答案】2H++2e-=H2↑ Cu2++2e-=Cu D>A>B>C 0.02
【解析】
第一个原电池中,A金属不断溶解,说明A易失电子而作负极,B作正极,越容易失电子的金属活动性越强,正极上氢离子得电子发生还原反应,电极反应式为:2H++2e-=H2↑;第二个原电池中,C的质量增加,说明C上的铜离子得电子发生还原反应而作正极,电极反应式为:Cu2++2e-=Cu,B为负极,B的金属性大于C;第三个原电池中,A上有气体产生,说明A上氢离子得电子发生还原反应,电极反应式为:2H++2e-=H2↑,D失电子作负极,所以D的活动性大于A;所以金属性强弱顺序是D>A>B>C;若装置(Ⅲ)中A极电极反应式为:2H++2e-=H2↑,标准状况下体积为224mL的H2物质的量为0.01mol,则转移电子的物质的量为0.02mol。

练习册系列答案
相关题目