题目内容
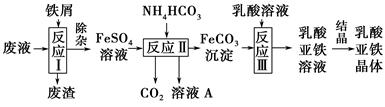
钴酸锂(LiCoO2)锂离子电池是一种应用广泛的新型电源,实验室尝试利用废旧钴酸锂锂离子电池回收铝、铁、铜、钴、锂元素,实验过程如下:
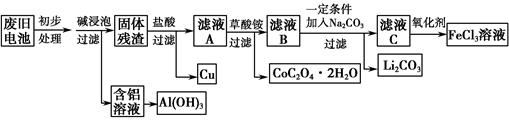
(1)碱浸泡过程中,铝被溶解的离子方程式为__________________________
(2)滤液A中加入草酸铵溶液,使Co元素以CoC2O4·2H2O沉淀形式析出。草酸钴是制备氧化钴及钴粉的重要原料。在空气中CoC2O4·2H2O的热分解失重数据见下表,请补充完整表中的热分解方程式。
(3)过滤Li2CO3时发现滤液中有少量浑浊,从实验操作的角度给出两种可能的原因:_____________________________________________________________
(4)最终所得的FeCl3溶液可作净水剂,试结合离子方程式解释其净水原理________________________________________________________

(1)碱浸泡过程中,铝被溶解的离子方程式为__________________________
(2)滤液A中加入草酸铵溶液,使Co元素以CoC2O4·2H2O沉淀形式析出。草酸钴是制备氧化钴及钴粉的重要原料。在空气中CoC2O4·2H2O的热分解失重数据见下表,请补充完整表中的热分解方程式。
| 序号 | 温度范围/℃ | 热分解方程式 | 固体失重率 |
| ① | 120~220 | | 19.67% |
| ② | 280~310 | | 56.10% |
(3)过滤Li2CO3时发现滤液中有少量浑浊,从实验操作的角度给出两种可能的原因:_____________________________________________________________
(4)最终所得的FeCl3溶液可作净水剂,试结合离子方程式解释其净水原理________________________________________________________
(1)2Al+2OH-+2H2O===2AlO2—+3H2↑
(2)①CoC2O4·2H2O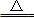 CoC2O4+2H2O ②3CoC2O4+2O2
CoC2O4+2H2O ②3CoC2O4+2O2 Co3O4+6CO2
Co3O4+6CO2
(3)玻璃棒下端靠在滤纸的单层处,导致滤纸破损;漏斗中液面高于滤纸边缘(其他合理答案亦可)
(4)Fe3+发生水解:Fe3++3H2O===Fe(OH)3(胶体)+3H2O,水解生成的Fe(OH)3具有吸附悬浮杂质的功能
(2)①CoC2O4·2H2O
 CoC2O4+2H2O ②3CoC2O4+2O2
CoC2O4+2H2O ②3CoC2O4+2O2 Co3O4+6CO2
Co3O4+6CO2(3)玻璃棒下端靠在滤纸的单层处,导致滤纸破损;漏斗中液面高于滤纸边缘(其他合理答案亦可)
(4)Fe3+发生水解:Fe3++3H2O===Fe(OH)3(胶体)+3H2O,水解生成的Fe(OH)3具有吸附悬浮杂质的功能
CoC2O4·2H2O在空气中加热首先想到是失去结晶水,根据固体失重率数据可判断120~220 ℃时结晶水全部失去。温度再升高,根据失重率可求得剩余固体为Co3O4,钴元素的价态发生变化,起氧化作用的应该是空气中的O2,由此可得化学方程式。

练习册系列答案
相关题目
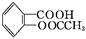 )是世界上应用最广泛的解热、镇痛和抗炎药。乙酰水杨酸受热易分解,分解温度为128~135 ℃。某学习小组在实验室以水杨酸(邻羟基苯甲酸)与醋酸酐[(CH3CO)2O]为主要原料合成阿司匹林,制备基本操作流程如下:
)是世界上应用最广泛的解热、镇痛和抗炎药。乙酰水杨酸受热易分解,分解温度为128~135 ℃。某学习小组在实验室以水杨酸(邻羟基苯甲酸)与醋酸酐[(CH3CO)2O]为主要原料合成阿司匹林,制备基本操作流程如下:
 粗产品
粗产品
 乙酰水杨酸
乙酰水杨酸 测熔点
测熔点
 乙酰水杨酸
乙酰水杨酸