题目内容
【题目】反应A(g)+B(g)![]() C(g)+D(g)过程中的能量变化如图所示,回答下列问题。
C(g)+D(g)过程中的能量变化如图所示,回答下列问题。
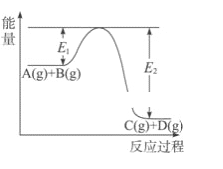
(1)该反应是___________反应(填“吸热”、“放热”)。
(2) 在反应体系中加入催化剂,化学反应速率增大,E1、E2和ΔH的变化是:E1________,E2_______,ΔH _______(填“增大”、“减小”或“不变”)
(3) 当反应达到平衡时,其他条件不变,升高温度,A的转化率______(填“增大”、“减小”或“不变”)。
【答案】放热 减小 减小 不变 减小
【解析】
(1)据图比较该反应的生成物总能量和反应物总能量大小;
(2)加入催化剂,会降低化学反应的活化能,但是焓变不会改变;
(3)当反应达到平衡时,其他条件不变,升高温度,平衡会向着吸热的方向移动。
(1)据图可知,该反应生成物总能量小于反应物总能量,是放热反应;
(2)由分析可知,加入催化剂,活化能降低,故E1减小,E2减小;焓变不会改变,故ΔH不变;
(3) 当反应达到平衡时,其他条件不变,升高温度,平衡会向着吸热的方向移动,即平衡会向着逆反应方向移动,所以A的转化率减小。

【题目】下表为元素周期表的一部分,根据表中所列出的元素回答下列问题。
族 周期 | IA | IIA | IIIA | IVA | VA | VIA | VIIA |
2 | a | b | c | d | |||
3 | e | f | g | h | i | j |
(1)f和d形成的物质的化学式为____。
(2)ac2分子的电子式为___。
(3)g单质溶于NaOH溶液的离子方程式为____。
(4)e单质在氧气中点燃得到淡黄色固体
①淡黄色固体的电子式为___,
②该物质存在的化学键的类型有___。
(5)为了比较该部分周素表中非金属元素的非金属性强弱,以下说法不正确的是___。
a.可以利用这些元素的最高价氧化物对应水化物的酸性比较这些元素的非金属性
b.已知j的气态氢化物水溶液的酸性比i的气态氢化物的水溶液酸性强,则非金属j>i
c.向i的气态氢化物的水溶液中加j单质,发现溶液变浑浊,则i的非金属性弱于j