题目内容
在密闭容器中,一定条件下进行如下反应NO(g)+CO(g)
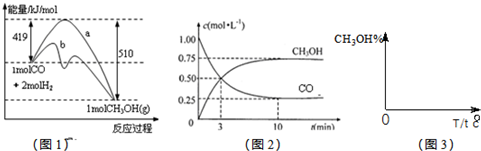
 N2(g)+CO2(g),ΔH=-373.2 kJ/mol,达到平衡后,为提高该反应的速率和NO的转化率,采取的正确措施是( )
N2(g)+CO2(g),ΔH=-373.2 kJ/mol,达到平衡后,为提高该反应的速率和NO的转化率,采取的正确措施是( )
A.加催化剂同时升高温度 B.加催化剂同时增大压强
C.升高温度同时充入N2 D.降低温度同时增大压强
【答案】
B
【解析】
试题分析:该反应的正反应是气体体积减小的放热反应。A.加催化剂能使化学反应速率加快,但升高温度根据平衡移动原理,化学平衡向吸热反应方向即向逆反应方向移动,NO的转化率降低。错误。B.加催化剂能使化学反应速率加快,同时增大压强根据平衡移动原理,化学平衡向气体体积减小的方向即正反应方向移动,NO的转化率提高。正确。C.升高温度化学反应速率加快,同时充入N2根据平衡移动原理:升高温度平衡逆向移动,增加生成物的浓度,平衡向逆反应方向移动,NO的转化率降低。错误。D.降低温度化学反应速率减慢,化学平衡正向移动,同时增大压强,平衡正向移动。由于温度对平衡的影响大于压强增大对平衡的影响,所以速率总的来说减慢。错误。
考点:考查外界条件对化学反应速率和化学平衡的移动的影响的知识。

练习册系列答案
相关题目

 联氨(N2H4)及其衍生物是重要的火箭燃料,N2H4与N2O4反应能放出大量的热.
联氨(N2H4)及其衍生物是重要的火箭燃料,N2H4与N2O4反应能放出大量的热.