题目内容
甲醇是一种可再生能源,具有广泛的开发和应用前景,因此甲醇被称为21世纪的新型燃料.工业上用CO生产燃料甲醇,一定条件下发生反应:CO(g)+2H2(g)?CH3OH(g).图l表示反应中能量的变化;图2表示一定温度下,在体积为2L的密闭容器中加入4mol H2和一定量的CO后,CO和CH3OH(g)的浓度随时间变化图.
请回答下列问题:
(1)在“图1”中,曲线
(2)根据“图2”判断,下列说法正确的是
a.起始充入的CO为1mol
b.增加CO浓度,可使H2的转化率增大
c.容器中压强恒定时,反应已达平衡状态
d.保持温度和密闭容器容积不变,再充入1molCO和2molH2,再次达到平衡时n(CH3OH)/n(CO)会增大
(3)从反应开始到建立平衡,v(H2)=
(4)请在“图3”中画出平衡时甲醇蒸气百分含量(纵坐标)随温度(横坐标)变化的曲线,要求画压强不同的2条曲线(在曲线上标出P1、P2,且P1>P2).

请回答下列问题:
(1)在“图1”中,曲线
b
b
(填“a”或“b”)表示使用了催化剂;该反应属于放热
放热
(填“吸热”或“放热”)反应.(2)根据“图2”判断,下列说法正确的是
bcd
bcd
a.起始充入的CO为1mol
b.增加CO浓度,可使H2的转化率增大
c.容器中压强恒定时,反应已达平衡状态
d.保持温度和密闭容器容积不变,再充入1molCO和2molH2,再次达到平衡时n(CH3OH)/n(CO)会增大
(3)从反应开始到建立平衡,v(H2)=
0.15moL/(L?min)
0.15moL/(L?min)
;该温度下CO(g)+2H2(g)?CH3OH(g)的化学平衡常数为12
12
.若保持其它条件不变,将反应体系升温,则该反应的化学平衡常数将减小
减小
(填“增大”、“减小”或“不变”).(4)请在“图3”中画出平衡时甲醇蒸气百分含量(纵坐标)随温度(横坐标)变化的曲线,要求画压强不同的2条曲线(在曲线上标出P1、P2,且P1>P2).
分析:(1)根据活化能的大小判断;根据反应物与生成物的总能量判断;
(2)反应方程式为CO(g)+2H2(g)?CH3OH(g),根据方程式结合图象进行判断;
(3)计算出CO的反应速率,结合方程式可计算氢气的反应速率,计算出平衡时各物质的浓度,可计算出平衡常数;正反应放热,升高温度平衡常数减小;
(4)根据压强对平衡移动的影响判断.
(2)反应方程式为CO(g)+2H2(g)?CH3OH(g),根据方程式结合图象进行判断;
(3)计算出CO的反应速率,结合方程式可计算氢气的反应速率,计算出平衡时各物质的浓度,可计算出平衡常数;正反应放热,升高温度平衡常数减小;
(4)根据压强对平衡移动的影响判断.
解答:解:(1)加入催化剂,可降低反应的活化能,由图象可知b活化能较低,应加入催化剂,反应物的总能量大于生成物的总能量,则反应为放热反应,
故答案为:b;放热;
(2)A.CO的起始浓度为1moL/L,体积为2L,则起始充入的CO为2mol,故a错误;
B.增加CO浓度,平衡向正方向移动,H2的转化率增大,故b正确;
C.由于反应前后气体的体积不等,则容器中压强恒定时,反应已达到平衡状态,故c正确;
D.保持温度和密闭容器容积不变,再充入1mol CO和2mol H2,相当于在原来的基础上缩小体积,压强增大,平衡向正反应方向移动,则平衡时
会增大,故d正确.
故答案为:bcd;
(3)从反应开始到建立平衡,v(CO)=
=0.075moL/(L?min),
则v(H2)=2v(CO)=0.15moL/(L?min),
平衡时:c(CO)=0.25mol/L,c(CH3OH)=0.75mol/L,
则消耗n(CO)=0.75mol/L×2L=1.5mol,消耗的n(H2)=3mol,
平衡时c(H2)=
=0.5mol/L,
k=
=12,
故答案为:0.15moL/(L?min);12;
(4)增大压强,平衡向正反应方向移动,则甲醇的百分含量增大,温度升高,平衡向逆反应方向移动,甲醇的百分含量降低,则图象可为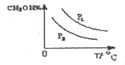 ,
,
故答案为: .
.
故答案为:b;放热;
(2)A.CO的起始浓度为1moL/L,体积为2L,则起始充入的CO为2mol,故a错误;
B.增加CO浓度,平衡向正方向移动,H2的转化率增大,故b正确;
C.由于反应前后气体的体积不等,则容器中压强恒定时,反应已达到平衡状态,故c正确;
D.保持温度和密闭容器容积不变,再充入1mol CO和2mol H2,相当于在原来的基础上缩小体积,压强增大,平衡向正反应方向移动,则平衡时
| n(CH3OH) |
| n(CO) |
故答案为:bcd;
(3)从反应开始到建立平衡,v(CO)=
| 1mol/L-0.25mol/L |
| 10min |
则v(H2)=2v(CO)=0.15moL/(L?min),
平衡时:c(CO)=0.25mol/L,c(CH3OH)=0.75mol/L,
则消耗n(CO)=0.75mol/L×2L=1.5mol,消耗的n(H2)=3mol,
平衡时c(H2)=
| 4mol-3mol |
| 2L |
k=
| 0.75 |
| 0.25×0.52 |
故答案为:0.15moL/(L?min);12;
(4)增大压强,平衡向正反应方向移动,则甲醇的百分含量增大,温度升高,平衡向逆反应方向移动,甲醇的百分含量降低,则图象可为
 ,
,故答案为:
 .
.点评:本题考查较为综合,涉及化学平衡的计算、化学平衡的移动以及影响因素、化学反应与能量变化等问题,题目难度中等,注意盖斯定律的运用以及化学平衡常数的意义.

练习册系列答案
 世纪百通期末金卷系列答案
世纪百通期末金卷系列答案
相关题目

 能源短缺是人类面临的重大问题.甲醇是一种可再生能源,具有广泛的开发和应用前景.
能源短缺是人类面临的重大问题.甲醇是一种可再生能源,具有广泛的开发和应用前景. (2012?红桥区一模)能源短缺是人类社会面临的重大问题.甲醇是一种可再生能源,具有广泛的开发和应用前景.
(2012?红桥区一模)能源短缺是人类社会面临的重大问题.甲醇是一种可再生能源,具有广泛的开发和应用前景.