题目内容
常温下,向l00mL0.01mol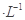 HA溶液中逐滴加入0.02mol
HA溶液中逐滴加入0.02mol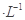 MOH溶液,如图所示曲线表示混合溶液的pH变化情况(溶液体积变化忽略不计)。下列说法中不正确的是:
MOH溶液,如图所示曲线表示混合溶液的pH变化情况(溶液体积变化忽略不计)。下列说法中不正确的是: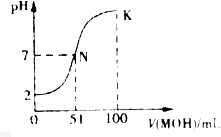
| A.HA为一元强酸 |
| B.MOH为一元弱碱 |
| C.N点水的电离程度小于K点水的电离程度 |
| D.若K点对应的溶液的PH=10,则有c(MOH)+ c(OH-)- c(H+)=0.005mol/L |
C
解析试题分析:由图像分析知加入碱的体积为51mL时溶液呈中性,说明二者不都是强电解质,若碱为强碱则加入碱50mL时恰好完全反应,此时为强碱弱酸盐,溶液应呈碱性,与图像不符,所以酸应为强酸,碱为弱碱。A、B正确;C、N点时,溶液呈中性,氢离子浓度等于氢氧根离子浓度=1×10-7mol/L,而K点时碱过量,抑制水的电离,所以N点水的电离程度大于K点水的电离程度,错误;D、在K点时加入碱的体积为100mL,此时溶液是MOH与MA等浓度的混合液且浓度都为0.005mol/L,根据物料守恒得c(MOH)+c(M+)="0.01" mol/L,根据电荷守恒得c(M+)+c(H+)=c(A-)+c(OH-),二式结合得
c(MOH)+ c(OH-)- c(H+)="0.01-" c(A-)=0.01-0.005=0.005mol/L,正确,答案选C。
考点:考查图像分析能力,酸碱混合液中守恒规律的应用,水的电离程度的比较

高氯酸、硫酸、硝酸和盐酸都是强酸,其酸性在水溶液中差别不大。以下是某温度下这四种酸在冰醋酸中的电离常数:从下表格中判断下列说法正确的是
| 酸 | HClO4 | H2SO4 | HCl | HNO3 |
| Ka | 1.6×10-5 | 6.3×10-9 | 1.6×10-9 | 4.2×10-10 |
A.在冰醋酸和水中这四种酸都没有完全电离
B.在冰醋酸中高氯酸是这四种酸中最弱的酸
C.在冰醋酸中硫酸的电离方程式为H2SO4=2H++SO42-
D.水对于这四种酸的强弱没有区分能力,但醋酸可以区别这四种酸的强弱
在pH都等于9的NaOH和CH3COONa两种溶液中,设由水电离产生的OH-离子浓度分别为A mol·L-1与B mol·L-1,则A和B的关系为
| A.A>B | B.A=10-4B | C.B=10-4A | D.A=B |
已知在25℃时,氯化银的Ksp=1.8×10-10,现将足量氯化银分别放入下列溶液中,相同温度下c(Ag+)最大的是
| A.100mL蒸馏水 | B.100mL 0.2mol·L-1 AgNO3 |
| C.100 mL 0.1mol·L-1AlCl3 | D.100mL 0.1 mol·L-1盐酸 |
下列能正确表示水解的离子方程式是
A.CH3COOH + H2O  CH3COO- + H3O+ CH3COO- + H3O+ |
B.NH4+ + H2O  NH3·H2O + H+ NH3·H2O + H+ |
C.CO32- + 2H2O H2CO3 + 2OH- H2CO3 + 2OH- |
D.Br- + H2O  HBr + OH- HBr + OH- |
在一定温度下,当Mg(OH)2固体在水溶液中达到下列平衡时:Mg(OH)2 Mg2++2OH-,要使Mg(OH)2固体减少而c(Mg2+)不变,可采取的措施是 ( )
Mg2++2OH-,要使Mg(OH)2固体减少而c(Mg2+)不变,可采取的措施是 ( )
| A.加MgSO4 | B.加HCl溶液 | C.加NaOH | D.加少量水 |
下列溶液一定呈中性的是 ( )。
| A.c(H+)=c(OH-)=10-6 mol·L-1的溶液 |
| B.pH=7的溶液 |
| C.使石蕊试液呈紫色的溶液 |
| D.酸与碱恰好完全反应生成正盐的溶液 |
室温下,在pH为5的NH4Cl溶液、pH为9的NaHCO3溶液和pH为5的盐酸中,水的电离度分别为:α1、α2、α3,它们之间的大小关系是 ( )
| A.α1<α2<α3 | B.α1=α2>α3 | C.α1>α2>α3 | D.无法判断 |