题目内容
12.汽车上的催化转化器,可将尾气中的主要污染物转化成无毒的物质,反应为:2NO(g)+2CO(g)?N2(g)+2CO2(g)△H=-746.6kJ/mol.某温度时,用气体传感器测得不同时间的NO和CO的浓度如下表:| 时间(s) | 0 | 1 | 2 | 3 | 4 | 5 |
| c(NO)(×10-4 mol/L) | 10 | 4.05 | 2.50 | 1.50 | 1.00 | 1.00 |
| c(CO)(×10-3 mol/L) | 3.60 | 3.05 | 2.85 | 2.75 | 2.70 | 2.70 |
| A. | 该反应转化较快,具有现实意义 | |
| B. | 催化转化器在冬季时对废气转化的效率比夏季更高 | |
| C. | 在该温度下,反应的平衡常数K=10000 | |
| D. | 2 s末的平均反应速率为v(NO)=3.75×10-4 mol•L-1•s-1 |
分析 该反应的正反应为放热反应,升高温度不利于平衡向正向移动,反应速率较快,可适用于废气的处理,计算出平衡时各物质的浓度,结合平衡常数表达式可计算平衡常数,以此解答该题.
解答 解:A.由表中数据可知,当反应至4s时,达到平衡状态,NO的浓度变化较大,说明反应转化较快,可用于尾气处理,故A正确;
B.该反应的正反应为放热反应,升高温度不利于平衡向正向移动,故B正确;
C.2NO(g)+2CO(g)=N2(g)+2CO2(g)
初始浓度:10×10-4 3.6×10-3 0 0
变化浓度:9×10-4 9×10-4 4.5×10-4 9×10-4
平衡浓度:1×10-4 2.7×10-3 4.5×10-4 9×10-4
K=$\frac{4.5×10{\;}^{-4}×(9×10{\;}^{-4}){\;}^{2}}{(1×10{\;}^{-4}){\;}^{2}×(2.7×10{\;}^{-3}){\;}^{2}}$=5000,故C错误;
D.2s内的平均反应速率v(NO)=$\frac{(10-2.5)×10{\;}^{-4}mol/L}{2s}$=3.75×10-4mol•L-1•S1,故D正确;
故选C.
点评 本题考查化学平衡的调控作用,侧重于学生的分析能力和计算能力的考查,为高考常见题型和高频考点,注意把握反应的特点以及影响因素的判断,难度不大.

练习册系列答案
 状元坊全程突破导练测系列答案
状元坊全程突破导练测系列答案
相关题目
2.欲从苯酚的乙醇溶液中回收苯酚,有下列操作:①蒸馏;②过滤;③分液;④加入足量的金属钠;⑤通入过量的CO2;⑥加入足量的NaOH溶液;⑦加入足量的FeCl3溶液;⑧加入足量浓溴水;⑨加入适量盐酸.合理的步骤是( )
| A. | ④⑤⑨ | B. | ⑥①⑤③ | C. | ⑧②⑦① | D. | ⑦①③④ |
3.汽车尾气(含烃类、CO、NO与SO2等)是城市主要污染源之一,治理的办法之一是在汽车排气管上装催化转化器,它使NO与CO反应生成可参与大气生态循环的无毒气体,其反应原理是:2NO(g)+2CO(g)═N2(g)+2CO2(g),在298K、100kPa下,△H=-113kJ•mol-1,△S=-145J•mol-1•K-1.下列说法中错误的是( )
| A. | 该反应中反应物的总能量高于生成物的总能量 | |
| B. | 该反应常温下不能自发进行,因此需要高温和催化剂 | |
| C. | 该反应常温下能自发进行,高温和催化剂只是加快反应的速率 | |
| D. | 汽车尾气中的这两种气体会与血红蛋白结合而使人中毒 |
20.下列反应中,属于加成反应的是( )
| A. | 乙烯使酸性KMnO4溶液褪色 | |
| B. | 将苯滴入溴水中,振荡后水层接近无色 | |
| C. | 乙烯使溴水褪色 | |
| D. | 甲烷与氯气混合,光照一段时间后黄绿色变浅 |
17.下列说法中,正确的是( )
| A. | 丙烯的结构简式可以表示为CH3CHCH2 | |
| B. | 用酒精可以将溴水中的溴萃取出来 | |
| C. | 乙烷、乙醇和乙酸都能发生取代反应 | |
| D. | 油脂都不能使酸性高锰酸钾溶液褪色 |
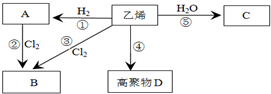 有机物A、B、C、D有如下转化关系.回答下列问题:
有机物A、B、C、D有如下转化关系.回答下列问题: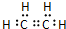 ,分子中含有的共价键类型有非极性键、极性键(填极性键或非极性键).
,分子中含有的共价键类型有非极性键、极性键(填极性键或非极性键). ,反应类型:加聚反应.
,反应类型:加聚反应.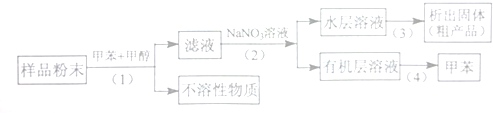
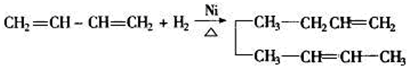
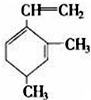 ,当它与等物质的量的Br2的水溶液发生加成反应时有多种产物,请补写除给出的两种结构外的其他三种产物的结构简式.
,当它与等物质的量的Br2的水溶液发生加成反应时有多种产物,请补写除给出的两种结构外的其他三种产物的结构简式.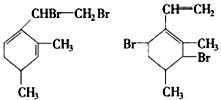
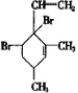
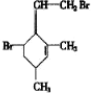
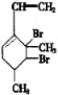 .
.