题目内容
7. 有机物A、B、C、D有如下转化关系.回答下列问题:
有机物A、B、C、D有如下转化关系.回答下列问题:(1)乙烯的电子式为
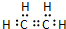 ,分子中含有的共价键类型有非极性键、极性键(填极性键或非极性键).
,分子中含有的共价键类型有非极性键、极性键(填极性键或非极性键).(2)写出反应的化学方程式和有机反应类型:
④
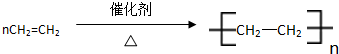 ,反应类型:加聚反应.
,反应类型:加聚反应.⑤CH2=CH2+H2O$\stackrel{一定条件}{→}$CH3CH2OH,反应类型:加成反应.
分析 乙烯与水发生加成反应生成C为CH3CH2OH,乙烯与氢气发生加成反应生成A为CH3CH3,乙烯与氯气发生加成反应生成B为ClCH2CH2Cl,乙烷与氯气发生取代反应可以得到ClCH2CH2Cl,乙烯发生加聚反应生成高聚物为 ,据此解答.
,据此解答.
解答 解:乙烯与水发生加成反应生成C为CH3CH2OH,乙烯与氢气发生加成反应生成A为CH3CH3,乙烯与氯气发生加成反应生成B为ClCH2CH2Cl,乙烷与氯气发生取代反应可以得到ClCH2CH2Cl,乙烯发生加聚反应生成高聚物为 .
.
(1)乙烯的电子式为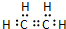 ,碳原子之间形成非极性键,碳原子与氢原子之间形成极性键,
,碳原子之间形成非极性键,碳原子与氢原子之间形成极性键,
故答案为: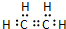 ;非极性键、极性键;
;非极性键、极性键;
(2)反应④的反应方程式为: ,属于加聚反应;
,属于加聚反应;
反应⑤的反应方程式为:CH2=CH2+H2O$\stackrel{一定条件}{→}$CH3CH2OH,属于加成反应,
故答案为: ;加聚反应;CH2=CH2+H2O$\stackrel{一定条件}{→}$CH3CH2OH;加成反应.
;加聚反应;CH2=CH2+H2O$\stackrel{一定条件}{→}$CH3CH2OH;加成反应.
点评 本题考查有机物推断,是烯烃的性质与转化,比较基础,有利于基础知识的巩固.

练习册系列答案
相关题目
18.由两种元素组成的化合物M有如下转化关系:

下列推断正确的是( )

下列推断正确的是( )
| A. | M可能是FeS2、Fe3C、CuS、和Fe3O4 | B. | Y可能是Fe(OH)3、Fe2O3 、Cu2O | ||
| C. | X溶液能溶解铁、铜等金属 | D. | 无色液体可能是N2O4和H2O |
15.雷美替胺是首个没有列为特殊管制的非成瘾失眠症治疗药物,合成该有机物过程中涉及如下转化,下列说法正确的是( )


| A. | 与化合物Ⅰ互为同分异构体,且分子中含有2个醛基的芳香族化合物有9种 | |
| B. | 化合物Ⅰ、Ⅱ、Ⅲ均能与NaHCO3溶液发生反应 | |
| C. | 化合物Ⅱ中共含有4种官能团 | |
| D. | 可用溴水区分化合物Ⅱ和化合物Ⅲ |
2.下列金属冶炼的反应原理,不正确的是( )
| A. | 2NaCl(熔融)$\frac{\underline{\;电解\;}}{\;}$2Na+Cl2↑ | B. | MgO+H2$\frac{\underline{\;\;△\;\;}}{\;}$Mg+H2O | ||
| C. | Fe2O3+3CO$\frac{\underline{\;高温\;}}{\;}$2Fe+3CO2 | D. | 2Ag2O$\frac{\underline{\;\;△\;\;}}{\;}$4Ag+O2↑ |
12.汽车上的催化转化器,可将尾气中的主要污染物转化成无毒的物质,反应为:2NO(g)+2CO(g)?N2(g)+2CO2(g)△H=-746.6kJ/mol.某温度时,用气体传感器测得不同时间的NO和CO的浓度如下表:
经分析,得出结论不正确的是( )
| 时间(s) | 0 | 1 | 2 | 3 | 4 | 5 |
| c(NO)(×10-4 mol/L) | 10 | 4.05 | 2.50 | 1.50 | 1.00 | 1.00 |
| c(CO)(×10-3 mol/L) | 3.60 | 3.05 | 2.85 | 2.75 | 2.70 | 2.70 |
| A. | 该反应转化较快,具有现实意义 | |
| B. | 催化转化器在冬季时对废气转化的效率比夏季更高 | |
| C. | 在该温度下,反应的平衡常数K=10000 | |
| D. | 2 s末的平均反应速率为v(NO)=3.75×10-4 mol•L-1•s-1 |
16.糖尿病人的尿液中常含有葡萄糖,某同学设计了如下荒谬的检验方法:让患者服下新制的碱性氢氧化铜悬浊液1 h后,再观察病人的尿液中是否会有红色沉淀物.你认为下列解释不合理的是( )
| A. | 服进肠胃的药剂根本不会直接进入人的膀胱中,Cu(OH)2悬浊液无法与葡萄糖作用 | |
| B. | 所用药剂具有毒性(含重金属元素Cu)和强腐蚀性(含NaOH),不能内服 | |
| C. | 该同学设计是正确的,但由于体温达不到令Cu(OH)2悬浊液与葡萄糖反应的温度,故检验不会成功 | |
| D. | 由于人们吃入的淀粉在体内也能水解成葡萄糖,会干扰检验的现象,检验应空腹进行 |
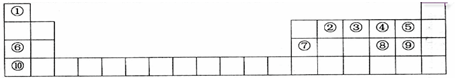
 ,其最高氧化物水化物与⑥号元素最高价氧化物水化物反应的离子方程式为Al(OH)3+OH-=[Al(OH)4]-_.
,其最高氧化物水化物与⑥号元素最高价氧化物水化物反应的离子方程式为Al(OH)3+OH-=[Al(OH)4]-_.