题目内容
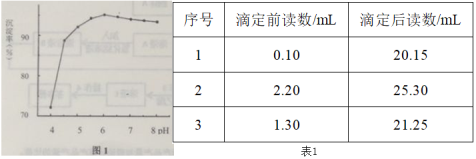
【题目】NaNO2可用作食品添加剂。测定粗产品中NaNO2的含量。称取m g粗产品,溶解后配制成250 mL溶液。取出25.00mL溶液,用cmolL-1酸性KMnO4溶液平行滴定三次,平均消耗的体积为V mL。
已知:2MnO4-+6H+ +5NO2-=5NO3-+2Mn2++3H2O
(1)配制溶液时,需使用的玻璃仪器除烧杯、玻璃棒外,还有___(填字母)。
A. 250 mL容量瓶 B. 量筒 C. 胶头滴管 D. 锥形瓶
(2)用____(填“酸式”或“碱式”)滴定管盛放高锰酸钾溶液。
(3)该实验___(填“需要”或“不需要”)加入指示剂。当观察到___时,滴定达到终点。
(4)粗产品中NaNO2的质量分数为____(用代数式表示)。
【答案】AC 酸式 不需要 滴入最后一滴KMnO4溶液后,溶液紫色褪去,且30s内不恢复原来颜色 ![]() %或
%或![]() ×100%
×100%
【解析】
(1)在配制溶液时,需要使用容量瓶进行操作,在使用容量瓶进行定容时,要用到胶头滴管,故应选AC;
(2)酸性高锰酸钾具有强氧化性,会氧化碱式滴定管的胶皮管,因此要使用酸式滴定管;
(3)因为高锰酸钾有颜色,故可以不加入指示剂,滴入最后一滴KMnO4溶液后,溶液紫色褪去,且30s内不恢复原来颜色,说明达到滴定终点;
(4)首先计算消耗的酸性![]() 溶液的物质的量:
溶液的物质的量:![]()
,对应消耗![]() 的物质的量:
的物质的量:![]() ,消耗
,消耗![]() 的质量:
的质量:![]()
,则粗产品中![]() 的质量分数为:
的质量分数为: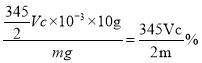 。
。

练习册系列答案
 课堂全解字词句段篇章系列答案
课堂全解字词句段篇章系列答案 步步高口算题卡系列答案
步步高口算题卡系列答案
相关题目