题目内容
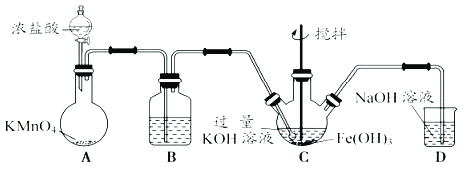
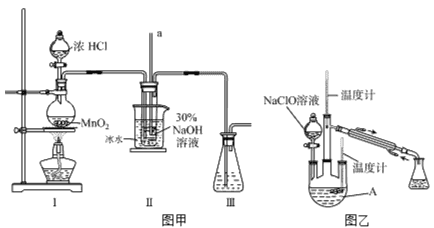
【题目】某化学研究性学习小组探究与铜有关的物质的性质,过程设计如下:
(提出猜想)
问题1:在周期表中,铜与铝的位置很接近,氢氧化铝具有两性,氢氧化铜有两性码?
问题2:铁和铜都有变价,一般情况下,Fe2+的稳定性小于的Fe3+,Cu+的稳定性也小于Cu2+吗?
问题3:硫酸铜溶液呈蓝色,铜与浓硝酸常温下反应生成的溶液也是蓝色吗?
(实验探究)
I. 解决问题1:
(1)实验需配制100mL 0.50mol·L-1 CuSO4溶液,除了天平、烧杯、玻璃棒、胶头滴管以外必需的玻璃仪器是______。
(2)为达到目的,某同学认为只要进行两次实验即可得出结论。请写出实验②的具体内容。
①向盛有CuSO4溶液的试管中滴加NaOH溶液至过量,观察生成的Cu(OH)2沉淀是否溶解;
②_______。
II. 解决问题2的实验步骤和现象如下:
①取一定量制得的氢氧化铜固体,于坩埚中灼烧,当温度达到80C~100C得到黑色固体粉末;继续加热至1000C以上,黑色粉末全部变成红色粉末氧化亚铜(Cu2O);
②取适量红色氧化亚铜粉末于洁净试管中,加入过量的稀硫酸,得到蓝色溶液,同时观察到试管底部还有红色固体存在。根据以上实验及现象:
(3)写出氧化亚铜与稀硫酸反应的离子方程式____________________________。
(4)从实验中可得出的结论是:当温度在1000C以上时________(填:Cu2+或Cu+,下同)稳定,在酸性溶液中________稳定。
III. 解决问题3,某同学设计的实验如下:取一铜片装入试管,加入适量的浓硝酸,观察溶液的颜色变化。
(5)另一同学认为此同学设计的实验有缺陷,原因是__________________________。
(6)铜与浓硝酸反应溶液呈绿色,有同学认为这是生成的NO2溶于其中的原因,并试图设计实验排除这种干扰。提出实验方案:向反应后的溶液中通入足量空气。试用化学反应方程式解释其原理:___________________________
【答案】100mL容量瓶 另取实验①中所得沉淀,滴加稀硫酸(或稀盐酸等)至过量,观察沉淀是否溶解 Cu2O + 2H+ =Cu + Cu2+ + H2O Cu+ Cu2+ 产生NO2气体,污染环境 4NO2+O2+2H2O=4HNO3
【解析】
(1)实验需配制100mL 0.50mol·L-1 CuSO4溶液,除了天平、烧杯、玻璃棒、胶头滴管以外必需有100mL容量瓶。答案:100mL容量瓶。
(2)要探究氢氧化铜是否具有两性,就要验证Cu(OH)2能否与强酸、强碱溶液反应。向CuSO4溶液加入的NaOH溶液,产生蓝色絮状沉淀。用试管取一定量的沉淀,继续滴加过量的NaOH溶液,观察生成的Cu(OH)2是否溶解;另取上述所得沉淀于试管中,滴加稀硫酸(或稀盐酸等)至过量,观察沉淀是否溶解。答案:另取实验所得沉淀,滴加稀硫酸(或稀盐酸等)至过量,观察沉淀是否溶解。
Ⅱ.(3)取适量红色氧化亚铜粉末于洁净试管中,加入过量的稀硫酸,得到蓝色溶液,同时观察到试管底部还有红色固体存在,说明氧化亚铜在酸性条件下发生歧化反应,生成单质铜和二价铜离子的盐溶液,离子方程式为:Cu2O + 2H+ =Cu + Cu2+ + H2O 。答案:Cu2O + 2H+ =Cu + Cu2+ + H2O。
(4)从实验中可得出的结论是:80C~100C 时,Cu2+稳定,1000C 以上Cu+稳定;在酸性环境Cu2+稳定,Cu+不稳定。答案:Cu+;Cu2+。
Ⅲ.(5)铜片装入试管,加入适量的浓硝酸,反应生成硝酸铜、水和二氧化氮气体,NO2有毒,不能排放到空气中,所以该同学设计的实验有缺陷。答案;产生NO2气体,污染环境。
(6)因为①3NO2+H2O=NO+2HNO3 ,②2NO+O2=2NO2, ①![]() 2+②: 4NO2+O2+2H2O=4HNO3,所以向反应后的溶液中通入足量空气,可以使NO2充分反应生成硝酸,减少干扰。答案:4NO2+O2+2H2O=4HNO3。
2+②: 4NO2+O2+2H2O=4HNO3,所以向反应后的溶液中通入足量空气,可以使NO2充分反应生成硝酸,减少干扰。答案:4NO2+O2+2H2O=4HNO3。