题目内容
【题目】(1)将0.3mol的气态高能燃料乙硼烷(B2H6)在氧气中燃烧,生成固态三氧化二硼和液态水,放出649.5kJ热量,该反应的热化学方程式为______________。又已知:H2O(g)=H2O(l);△H2=-44.0kJ/mol,则11.2L(标准状况)乙硼烷完全燃烧生成气态水时放出的热量是_____________kJ。
(2)已知:2NO2(g)![]() N2O4(g)ΔH1 2NO2(g)
N2O4(g)ΔH1 2NO2(g)![]() N2O4(l)ΔH2
N2O4(l)ΔH2
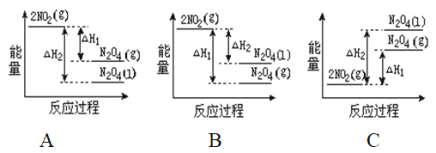
下列能量变化示意图中,正确的是(选填字母)_____________。
(3)依据盖斯定律可以对某些难以通过实验直接测定的化学反应的焓变进行推算。
已知:C(s,石墨)+O2(g)=CO2(g) ΔH1=-393.5 kJ·mol-1
2H2(g)+O2(g)=2H2O(l) ΔH2=-571.6 kJ·mol-1
2C2H2(g)+5O2(g)=4CO2(g)+2H2O(l) ΔH3=-2 599 kJ·mol-1
根据盖斯定律,计算298 K时由C(s,石墨)和H2(g)生成1 mol C2H2(g)反应的焓变(列出简单的计算式):___________________________。
(4)甲醇是一种新型的汽车动力燃料,工业上可通过CO和H2化合来制备甲醇气体(结构简式为CH3OH)。 已知某些化学键的键能数据如下表:
化学键 | C—C | C—H | H—H | C—O | C≡O | H—O |
键能/kJ·mol-1 | 348 | 413 | 436 | 358 | 1072 | 463 |
已知CO中的C与O之间为叁键连接,则工业制备甲醇的热化学方程式为_________。
【答案】B2H6(g)+3O2(g)=B2O3(s)+3H2O(l) △H=-2165kJ/mol 1016.5kJ A ΔH=(4ΔH1+ΔH2—ΔH3)÷2=+226.7kJmol-1 CO(g)+2H2(g)![]() CH3OH(g) △H=-116 kJ/mol
CH3OH(g) △H=-116 kJ/mol
【解析】
(1)0.3mol气态高能燃料乙硼烷在氧气中燃烧,生成固态三氧化二硼和液态水,放出649.5kJ的热量,则1mol气态高能燃料乙硼烷在氧气中燃烧,生成固态三氧化二硼和液态水,放出2165kJ的热量,反应的热化学方程式为:B2H6(g)+3O2(g)=B2O3(s)+3H2O(l)△H=-2165kJ/mol;①B2H6(g)+3O2(g)=B2O3(s)+3H2O(l)△H=-2165kJ/mol,②H2O(l)→H2O(g) △H=+44kJ/moL,由盖斯定律可知①+②×3得:B2H6(g)+3O2(g)=B2O3(s)+3H2O(g)△H=-2033kJ/mol,11.2L(标准状况)即0.5mol乙硼烷完全燃烧生成气态水时放出的热量是2033kJ/mol×0.5mol=1016.5kJ;
(2)降低温度,将NO2(g)转化为N2O4(l)说明反应2NO2(g)![]() N2O4(l)为放热反应,所以在图象中该反应的反应物的总能量比生成物的总能量高,同种物质气态变液态会放出热量,即液态时能量比气态时能量低,则N2O4(l)具有的能量比N2O4(g)具有的能量低,图象A符合,故A正确;故答案为:A。
N2O4(l)为放热反应,所以在图象中该反应的反应物的总能量比生成物的总能量高,同种物质气态变液态会放出热量,即液态时能量比气态时能量低,则N2O4(l)具有的能量比N2O4(g)具有的能量低,图象A符合,故A正确;故答案为:A。
(3)已知:①C(s,石墨)+O2(g)=CO2(g) ΔH1=-393.5 kJ·mol-1;②2H2(g)+O2(g)=2H2O(l) ΔH2=-571.6 kJ·mol-1;③2C2H2(g)+5O2(g)=4CO2(g)+2H2O(l) ΔH3=-2 599 kJ·mol-1,根据盖斯定律,①×4+②-③得到反应的热化学方程式为:4C(s,石墨)+2H2(g)=2C2H2(g) △H=+453.4kJmol-1,因此热化学方程式为:2C(s,石墨)+H2(g)=C2H2(g) △H=+226.7kJmol-1;
(4)CO(g)+2H2(g)![]() CH3OH(g),焓变=反应物总键能之和-生成物总键能之和,△H1=1072kJ/mol+2×436kJ/mol-(3×413kJ/mol+358kJ/mol+463kJ/mol)=-116
CH3OH(g),焓变=反应物总键能之和-生成物总键能之和,△H1=1072kJ/mol+2×436kJ/mol-(3×413kJ/mol+358kJ/mol+463kJ/mol)=-116 ![]() CH3OH(g)△H=-116 kJmol-1。
CH3OH(g)△H=-116 kJmol-1。