题目内容
【题目】工业中很多重要的化工原料都来源于石油化工,如图中的苯、丙烯、有机物A等,其中A的年产量可以用来衡量一个国家的石油化工发展水平。请回答下列问题:
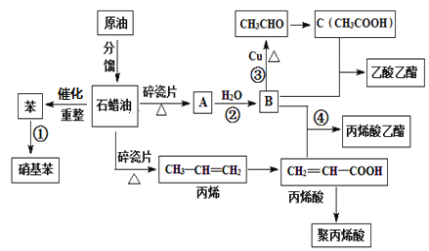
(1)A的结构简式为_______,丙烯酸中含氧官能团的名称为______;
(2)写出下列反应的反应类型①________,④________;
(3)下列说法正确的是:________;
A.为除去硝基苯中混有的浓HNO3和H2SO4,可将其倒入到NaOH溶液中,静置,分液
B.除去乙酸乙酯中的乙酸,加NaOH溶液、分液
C.有机物C与丙烯酸属于同系物
(4)写出④的反应方程式:__________。
【答案】CH2=CH2 羧基 硝化反应或取代反应 取代(或酯化)反应 A CH2=CHCOOH + CH3CH2OH![]() CH2=CHCOOCH2CH3+ H2O
CH2=CHCOOCH2CH3+ H2O
【解析】
A的产量可以用来衡量一个国家的石油化工发展水平,A应为CH2=CH2,乙烯与水发生加成反应生成乙醇,乙醇被催化氧化生成乙醛,乙醛进一步被氧化生成乙酸;乙醇和乙酸发生酯化反应生成乙酸乙酯。结合有机物的结构特点及反应类型进行判断分析。
(1)A为乙烯,其结构简式为CH2=CH2;丙烯酸中含氧官能团的名称为羧基;
(2)反应①是苯在浓硫酸催化下与浓硝酸发生硝化反应生成硝基苯和水,反应类型为硝化反应或取代反应;
反应④是乙醇和丙烯酸的酯化反应,反应类型为取代(或酯化)反应;
(3)A.浓HNO3和H2SO4与NaOH溶液反应,形成水层,硝基苯为有机层,静置,分液,选项A正确;
B.乙酸乙酯与氢氧化钠能反应,除去乙酸乙酯中的乙酸,应该用饱和碳酸钠溶液,选项B错误;
C.C是乙酸为饱和酸,丙烯酸为不饱和酸,两者结构不同,不是同系物,选项C错误;
综上所述答案为A;
(4)反应④是乙醇和丙烯酸的酯化反应,反应方程式为CH2=CHCOOH+CH3CH2OH![]() CH2=CHCOOCH2CH3+H2O。
CH2=CHCOOCH2CH3+H2O。

 期末好成绩系列答案
期末好成绩系列答案 99加1领先期末特训卷系列答案
99加1领先期末特训卷系列答案 百强名校期末冲刺100分系列答案
百强名校期末冲刺100分系列答案 好成绩1加1期末冲刺100分系列答案
好成绩1加1期末冲刺100分系列答案 金状元绩优好卷系列答案
金状元绩优好卷系列答案【题目】一定温度下,在三个体积均为0.5 L的恒容密闭容器中发生反应:CO(g)+Cl2(g)![]() COCl2(g),其中容器Ⅰ中反应在5 min时达到平衡状态。
COCl2(g),其中容器Ⅰ中反应在5 min时达到平衡状态。
容器编号 | 温度/℃ | 起始物质的量/mol | 平衡物质的量/mol | ||
CO | Cl2 | COCl2 | COCl2 | ||
Ⅰ | 500 | 1.0 | 1.0 | 0 | 0.8 |
Ⅱ | 500 | 1.0 | a | 0 | 0.5 |
Ⅲ | 600 | 0.5 | 0.5 | 0.5 | 0.7 |
下列说法中正确的是
A. 容器Ⅰ中前5 min的平均反应速率v(CO)=0.16 mol·L-1·min-1
B. 该反应正反应为吸热反应
C. 容器Ⅱ中起始时Cl2的物质的量为0.55 mol
D. 若起始时向容器Ⅰ加入CO0.8mol、Cl20.8mol,达到平衡时CO转化率大于80%