��Ŀ����
5����������ˮ�е����ʺ��ݼ����룮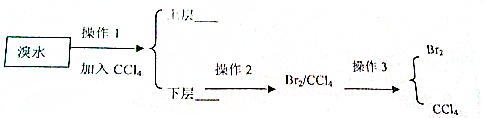
��1������1�IJ�������Ϊ��ȡ��������Ҫ����������̨������Ȧ����С�ձ�����Һ©������������ʹ��ǰҪ����Ƿ�©ˮ��
��2������1���ã�Һ���Ϊ���㣬�ϲ�Ϊ��Һ������ɫ���²�ΪҺ�ʳȺ�ɫ����������
��3������2������Ϊ��Һ������3������Ϊ����
��4������3�У�����Ҫ����Ӧ�����м������Ƭ��Ŀ���Ƿ�ֹ��ֹҺ���ٷУ�
��5�������ѡ��CCl4��ȡ��ˮ�����ԭ��
���� ����ˮ�м������Ȼ�̼�����Ȼ�̼�ܽ���ˮ�е�����ȡ��������Һ���ֲַ㣬���ܽ���Ȼ�̼�У����Ȼ�̼���ܶȴ���ˮ���پ�����Һ���õ��ϲ�Ϊˮ�㣬��Һ����Ϊ��ɫ��������Ȼ�̼��Һ���²㣬��Һ�ʳȺ�ɫ��������Ȼ�̼��Һ�ӷ�Һ©�����¿ڷų�����������Ȼ�̼��Һ��������ɵ�������Ȼ�̼���ݴ˴��⣻
��� �⣺����ˮ�м������Ȼ�̼�����Ȼ�̼�ܽ���ˮ�е�����ȡ��������Һ���ֲַ㣬���ܽ���Ȼ�̼�У����Ȼ�̼���ܶȴ���ˮ���پ�����Һ���õ��ϲ�Ϊˮ�㣬��Һ����Ϊ��ɫ��������Ȼ�̼��Һ���²㣬��Һ�ʳȺ�ɫ��������Ȼ�̼��Һ�ӷ�Һ©�����¿ڷų�����������Ȼ�̼��Һ��������ɵ�������Ȼ�̼��
��1������1�IJ�������Ϊ��ȡ��������Ҫ����������̨������Ȧ����С�ձ�����Һ©������Һ©����ʹ��ǰҪ����Ƿ�©ˮ��
�ʴ�Ϊ����ȡ����Һ©����©ˮ��
��2������1���ã�Һ���Ϊ���㣬�ϲ���Һ������ɫ���²���Һ�ʳȺ�ɫ��
�ʴ�Ϊ����Һ������ɫ��Һ�ʳȺ�ɫ��
��3������2�ǵõ�������Ȼ�̼��Һ������������Ϊ��Һ������3�Ƿ�����������Ȼ�̼��Һ������Һ�廥�ܣ����е㲻ͬ�����Բ���3������Ϊ����
�ʴ�Ϊ����Һ������
��4������ʱ��������ƿ�м������Ƭ��Ŀ���Ƿ�ֹҺ���ٷУ�
�ʴ�Ϊ����ֹҺ���ٷУ�
��5���������Ȼ�̼�е��ܽ��ԶԶ������ˮ�е��ܽ�ȣ������Ȼ�̼��ˮ�����ܣ����Կ�����CCl4��ȡ��ˮ���壬
���������Ȼ�̼�е��ܽ��ԶԶ������ˮ�е��ܽ�ȣ������Ȼ�̼��ˮ�����ܣ�
���� ������Ҫ���������ʵķ������ᴿ��Ҫѧ������������ȡ�ͷ�Һ�IJ���Ҫ�㣬�ѶȲ���ע��ʵ�����������������ã�

 ��������һ���þ�ϵ�д�
��������һ���þ�ϵ�д� Сѧ��10����Ӧ����ϵ�д�
Сѧ��10����Ӧ����ϵ�д���ش��������⣺
��1��ú����������Ҫ��ѧ��Ӧ����ʽΪ��C+H2O$\frac{\underline{\;����\;}}{\;}$CO+H2��
��2��ú�����������в������к�����H2S��Na2CO3��Һ���գ�����������ʽ�Σ��÷�Ӧ�Ļ�ѧ����ʽΪ��H2S+Na2CO3�TNaHS+NaHCO3��
��3������ˮú���ϳɶ����ѵ�������Ӧ���£�
��2H2��g��+CO��g���TCH3OH��g������H=-90.8kJ•mol-1
��2CH3OH��g���TCH3OCH3��g��+H2O��g������H=-23.5kJ•mol-1
��CO��g��+H2O��g���TCO2��g��+H2��g������H=-41.3kJ•mol-1
�ܷ�Ӧ��3H2��g��+3CO��g���TCH3OCH3��g��+CO2 ��g���ġ�H=-246.4kJ•mol-1��
һ�������µ��ܱ������У����ܷ�Ӧ�ﵽƽ�⣬Ҫ���CO��ת���ʣ����Բ�ȡ�Ĵ�ʩ��ce������ĸ���ţ���
a�����¸�ѹ b��������� c������CO2��Ũ�� d������CO��Ũ�� e�������������
��4����֪��Ӧ��2CH3OH��g���TCH3OCH3��g��+H2O��g��ij�¶��µ�ƽ�ⳣ��Ϊ400�����¶��£����ܱ������м���CH3OH����Ӧ��ijʱ�̲�ø���ֵ�Ũ�����£�
| ���� | CH3OH | CH3OCH3 | H2O |
| Ũ��/��mol•L-1�� | 0.44 | 0.6 | 0.6 |
��������CH3OH��10min��Ӧ�ﵽƽ�⣬��ʱc��CH3OH��=0.04mol/L��
| A�� | 2��3һ�������� | B�� | 3-��-1-��ϩ | ||
| C�� | ����ױ� | D�� | 4��4-����-1-��Ȳ |
| A�� | �÷�Ӧ�����û���Ӧ | B�� | ��ԭ�� I2��Cl2 | ||
| C�� | �ǽ�����Cl��I | D�� | ������ I2��Cl2 |
| A�� | ��ϩ����Ϊ����ˮ�����ʻ��������ڼ� | |
| B�� | ��Ȳȼ��ʱ�����¶ȸߣ���Ȳ������ں��ӻ��и���� | |
| C�� | ��ȩ��ˮ��Һ-�������ֿ�����ɱ�������� | |
| D�� | �Ҵ���������ȡ��ˮ�е��嵥�� |
| A�� | ͨ�����������۲�������ɫ������ | |
| B�� | ��������Һ�м���NaOH��Һ | |
| C�� | ��������Һ�м���KSCN��Һ | |
| D�� | ��������Һ�м�����ˮ���ټ���KSCN��Һ |
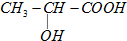 �������ι㷺Ӧ����ʳƷ��ҽҩ��������������һ���Ʊ����᷽�����£�
�������ι㷺Ӧ����ʳƷ��ҽҩ��������������һ���Ʊ����᷽�����£�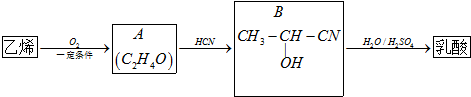
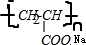 ��
��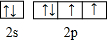 ����Ԫ�ص�����������
����Ԫ�ص�����������