��Ŀ����
15����������һ����Ҫ�����ȼ�ϣ�Ҳ�������������������ȣ��Գ��������ƻ����ã���ҵ�Ͽ�����ú���������ˮú�����ϳɶ����ѣ���ش��������⣺
��1��ú����������Ҫ��ѧ��Ӧ����ʽΪ��C+H2O$\frac{\underline{\;����\;}}{\;}$CO+H2��
��2��ú�����������в������к�����H2S��Na2CO3��Һ���գ�����������ʽ�Σ��÷�Ӧ�Ļ�ѧ����ʽΪ��H2S+Na2CO3�TNaHS+NaHCO3��
��3������ˮú���ϳɶ����ѵ�������Ӧ���£�
��2H2��g��+CO��g���TCH3OH��g������H=-90.8kJ•mol-1
��2CH3OH��g���TCH3OCH3��g��+H2O��g������H=-23.5kJ•mol-1
��CO��g��+H2O��g���TCO2��g��+H2��g������H=-41.3kJ•mol-1
�ܷ�Ӧ��3H2��g��+3CO��g���TCH3OCH3��g��+CO2 ��g���ġ�H=-246.4kJ•mol-1��
һ�������µ��ܱ������У����ܷ�Ӧ�ﵽƽ�⣬Ҫ���CO��ת���ʣ����Բ�ȡ�Ĵ�ʩ��ce������ĸ���ţ���
a�����¸�ѹ b��������� c������CO2��Ũ�� d������CO��Ũ�� e�������������
��4����֪��Ӧ��2CH3OH��g���TCH3OCH3��g��+H2O��g��ij�¶��µ�ƽ�ⳣ��Ϊ400�����¶��£����ܱ������м���CH3OH����Ӧ��ijʱ�̲�ø���ֵ�Ũ�����£�
| ���� | CH3OH | CH3OCH3 | H2O |
| Ũ��/��mol•L-1�� | 0.44 | 0.6 | 0.6 |
��������CH3OH��10min��Ӧ�ﵽƽ�⣬��ʱc��CH3OH��=0.04mol/L��
���� ��1��ú����������Ϊ��ú��ˮ������Ӧ����һ����̼��������
��2��H2S����Na2CO3��Һ���գ�������������ʽ�Σ����������Ƕ�Ԫ�ᣬ̼�������Ϊ��Ԫ�����������������ɵ�������ʽ��ΪNaHS��NaHCO3����ƽ��д��ѧ����ʽ��
��3�����ݸ�˹���ɣ�����֪����ʽ���εõ�Ŀ�귽��ʽ���ʱ�ֵ����Ӧ���㣬�ݴ˼��㷴Ӧ�ʱ䣻
Ҫ���CO��ת���ʣ�Ӧʹƽ��������Ӧ�ƶ���
3H2��g��+3CO��g���TCH3OCH3��g��+CO2��g�� ��Ӧ�ص�Ϊ������ӦΪ����ϵ����С�ķ�Ӧ����Ӧ�ʱ�С��0��˵����ӦΪ���ȷ�Ӧ��Ҫʹƽ��������Ӧ�ƶ������Բ�ȡ��ʩ������ѹǿ�������¶ȣ���С������Ũ�ȣ�����Ӧ��Ũ�ȣ�ʹ�ô������ܸı�ƽ��״̬��
��4���ټ���Qc������Qc��K�Ĵ�С��ϵ�жϷ�Ӧ���з����ж����淴Ӧ���ʣ�
����������ʽ����ƽ��ʱ�����Ũ�ȣ�����ƽ�ⳣ��������
��� �⣺��1��ú����������Ҫ��ѧ��Ӧ����ʽ��C+H2O$\frac{\underline{\;����\;}}{\;}$CO+H2��
�ʴ�Ϊ��C+H2O$\frac{\underline{\;����\;}}{\;}$CO+H2��
��2��ú�����������в������к�����H2S����Na2CO3��Һ���գ�������������ʽ�Σ�˵����Ӧ����Ϊ���⻯�ƺ�̼�����ƣ���Ӧ�Ļ�ѧ����ʽΪ��H2S+Na2CO3�TNaHS+NaHCO3��
�ʴ�Ϊ��H2S+Na2CO3�TNaHS+NaHCO3��
��3����2H2��g��+CO��g���TCH3OH��g������H=-90.8kJ•mol-1
��2CH3OH��g���TCH3OCH3��g��+H2O��g������H=-23.5kJ•mol-1
��CO��g��+H2O��g���TCO2��g��+H2��g������H=-41.3kJ•mol-1��
�ɸ�˹����֪���١�2+��+�ۣ����õ�3H2��g��+3CO��g��?CH3OCH3��g��+CO2 ��g����
���ԡ�H=2��H1+��H2+��H3=-246.4kJ•mol-1��
�ʴ�Ϊ��-246.4kJ•mol-1��
a������Ӧ���ȣ����¶ȿ�ʹƽ�����������ƶ�����a��ѡ��
b��ʹ�ô�����������ƽ����ƶ����������CO��ת���ʣ���b��ѡ��
c������CO2��Ũ�ȣ�����С������Ũ�ȣ�ƽ�����������ƶ����������COת���ʣ���cѡ��
d������CO��Ũ�ȣ�CO��ת���ʽ��ͣ���d��ѡ��
e������������ѣ�����С������Ũ�ȣ�ƽ�����������ƶ����������COת���ʣ���eѡ��
��ѡ��ce��
��4���ٷ�ӦŨ����Qc=$\frac{0.6mol/L��0.6mol/L}{��0.44mol/L��^{2}}$=1.86���¶��µ�ƽ�ⳣ��Ϊ400������Qc��K����Ӧ����������У���������Ӧ���ʴ����淴Ӧ���ʣ�
�ʴ�Ϊ������
����ƽ��ʱ������ˮ��Ũ��Ϊx����
2CH3OH��g���PCH3OCH3��g��+H2O��g��
ijʱ��Ũ�ȣ�mol•L-1����0.44 0.6 0.6
ת��Ũ�ȣ�mol•L-1����2x x x
ƽ��Ũ�ȣ�mol•L-1����0.44-2x 0.6+x 0.6+x
K=$\frac{��0.6+x��{\;}^{2}}{��0.44-2x��^{2}}$=400�����x=0.2mol/L��
����ƽ��ʱc��CH3OH��=0.44mol/L-0.2mol/L��2=0.04mol/L��
�ʴ�Ϊ��0.04mol/L��
���� ����Ϊ�ۺ��⣬�����˷���ʽ����д����Ӧ�ȵļ��㡢��ѧƽ���ƶ���Ӱ�����ء���ѧƽ�ⳣ����Ӧ�ã���ȷ��˹���ɼ��㷴Ӧ�ȵķ�������Ϥ��ѧƽ���ƶ����ɼ�ƽ�ⳣ����Ӧ���ǽ���ؼ�����Ŀ�Ѷ��еȣ�

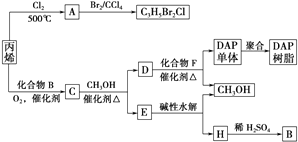
 ֥�鿪���γ�������ϵ�д�
֥�鿪���γ�������ϵ�д�| A�� | ������ | B�� | 1��2-������ | C�� | 1��3-������ | D�� | �Ҷ��� |
| 25��ʱ | pHֵ |
| ����H2S��Һ | 3.9 |
| SnS������ȫ | 1.6 |
| FeS��ʼ���� | 3.0 |
| FeS������ȫ | 5.5 |
A��KSCN��Һ B��NaOH��Һ C��KMnO4��Һ D��������Һ
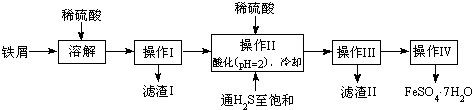
��2������II�У�ͨ�����������͵�Ŀ���dz�ȥ��Һ�е�Sn2+���ӣ�����ֹFe2+������������Һ���������ữ��pH=2��Ŀ���Ƿ�ֹFe2+�������ɳ�����
��3������IV�õ����̷�������������ˮϴ�ӣ���Ŀ���ǣ��ٳ�ȥ������渽�ŵ���������ʣ��ڽ���ϴ�ӹ�����FeSO4•7H2O����ģ�
��4���ⶨ�̷���Ʒ��Fe2+�����ķ����ǣ�a����ȡ2.850g�̷���Ʒ���ܽ⣬��250mL����ƿ�ж��ݣ�b����ȡ25.00mL������Һ����ƿ�У�c���������ữ��0.01000mol/LKMnO4��Һ�ζ����յ㣬����KMnO4��Һ�����ƽ��ֵΪ20.00mL��
�ٵζ�ʱ������Ӧ�����ӷ���ʽΪMnO4-+5Fe2++8H+=Mn2++5Fe3++4H2O��
���жϴ˵ζ�ʵ��ﵽ�յ�ķ����ǵμ����һ��KMnO4��Һʱ����Һ���dz��ɫ�Ұ�����ڲ���ɫ��
�ۼ���������Ʒ��FeSO4•7H2O����������Ϊ97.54%��
��������ʱ�����߸���Һ�棬����õ�FeSO4•7H2O����������ƫ�ߣ����ƫ�ߡ�����ƫ�͡�������Ӱ�족
| A�� | 25��ʱ��pH=13��1.0L Ba��OH��2��Һ�к��е�Ba2+��ĿΪ0.05NA | |
| B�� | ��״���£�2.24L CH2Cl2ֻ���е�C-Cl������ĿΪ0.2NA | |
| C�� | 1.8g��ˮ��D2O��ֻ����NA������ | |
| D�� | ���³�ѹ�£�21g��ϩ�뻷����Ļ�����к���ԭ����ĿΪ3NA |
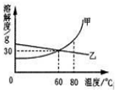 �±��г��˹�������A�ڲ�ͬ�¶�ʱ���ܽ�ȣ�
�±��г��˹�������A�ڲ�ͬ�¶�ʱ���ܽ�ȣ�| �¶�/�� | 0 | 10 | 20 | 30 | 40 | 50 | 60 | 70 | 80 | 90 |
| �ܽ��/g | 36 | 35 | 34 | 33 | 32 | 31 | 30 | 29 | 28 | 27 |
��2��ͨ�����ϱ����ݵķ���������A���ܽ������Ӧ��ͼ�е��ң���ס����ҡ�����
��3��80��ʱ������һ���������ʵ���Һ�����併�µ�60�棬�Ƿ��й�����������ȷ������С�����û�С���ȷ��������
 ��
��
 ����β������ɿ�����Ⱦ��ԭ��֮һ��������Ԫ�����еĴ�������ǿ����β���� CO��C��H����NO��������Ļ��ԣ�ʹ�������Ӧ��������Ⱦ�����ȥ��
����β������ɿ�����Ⱦ��ԭ��֮һ��������Ԫ�����еĴ�������ǿ����β���� CO��C��H����NO��������Ļ��ԣ�ʹ�������Ӧ��������Ⱦ�����ȥ��