题目内容
【题目】苯甲酸广泛用于医药、食品、染料、化工等领域。以下是实验室制备苯甲酸的一种方法。反应原理:
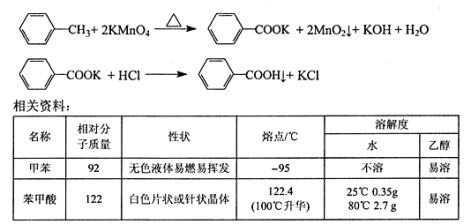

实验步骤:
①下图组装反应装置(冷凝水、夹持及加热装置未画出),并在三颈烧瓶中依次加入120mL水、稍过量高锰酸钾和3.0mL甲苯(密度为0.866g/ mL)。
②将三颈烧瓶中的混合液体搅拌、加热至沸腾,直到甲苯完全反应。
③趁热过滤反应混合物。若滤液呈紫色,则需加入适量的亚硫酸氢钠溶液至紫色褪去后再过滤,用热水洗涤滤渣,洗涤液合并至滤液中。
④用冰水冷却滤液,然后用浓盐酸酸化,过滤,用少量冷水洗涤滤渣,得到苯甲酸粗产品,经重结晶得到精制的苯甲酸。
回答下列问题:
(1)仪器 a名称为 。
(2)判断甲苯己完全反应的现象是 、回流液不再出现油珠。
(3)实验步骤④中,用少量冷水而不用热水洗涤滤渣的目的是 ;苯甲酸粗产品除了可用重结晶法精制外,还可用 法。
(4)精制的苯甲酸纯度测定:称取1.220g样品,用稀乙醇溶解并配成100 mL溶液,分别取25.00mL溶液,用0.1000 mo1·L-1NaOH标准溶液滴定,三次滴定消耗NaOH溶液的体积分别为V1=22.48mL.V2=22.52 mL.V3= 23.80mL。
①配制溶液时用稀乙醇而不用蒸馏水作溶剂的原因是 。
②若用酚酞作指示剂,确定滴定终点的现象是 。
③产品的纯度为 。
【答案】(1)(蛇形)冷凝管
(2)三颈烧瓶中混合液不再分层(或甲苯层消失)
(3)减少苯甲酸因溶解造成损失,升华
(4)①常温下苯甲酸微溶于水而易溶于乙醇②滴加最后一滴氢氧化钠标准溶液后,溶液由无色变为浅红色,且30秒不褪色③90%(3分)
【解析】
试题分析:(1)根据仪器的特征,仪器 a名称为(蛇形)冷凝管。
(2)因为甲苯不溶于水,但苯甲酸能溶于水,所以甲苯完全反应的现象为三颈烧瓶中混合液不再分层(或甲苯层消失)。
(3)因为苯甲酸能溶于水,所以用少量冷水可以减少苯甲酸因溶解造成损失,因为苯甲酸能升华,所以可以采用升华的方法分离。
(4)①常温下苯甲酸微溶于水而易溶于乙醇,所以配制溶液时用稀乙醇不用蒸馏水。②用酚酞做指示剂,滴定终点的现象为滴加最后一滴氢氧化钠标准溶液后,溶液由无色变为浅红色,且30秒不褪色。③V3数据与其他的数据差距大,所以舍去,求体积平均值为22.50毫升,所以纯度=4×22.50×0.1×122/(25×1.22)=90.00%。

 阅读快车系列答案
阅读快车系列答案【题目】除去下列物质中的杂质,所用试剂和方法不正确的是( )
物质 | 杂质 | 除杂所用试剂和方法 | |
A | KCl溶液 | I2 | 酒精,萃取 |
B | KNO3 | K2SO4 | Ba(NO3)2溶液,过滤 |
C | Cu | CuO | 盐酸,过滤 |
D | CaCO3 | CaO | H2O,过滤 |