��Ŀ����
����Ŀ��������ѧ֪ʶ�ش��������⣺
(1)������98%��Ũ����������������Ϊ20%��ϡ���ᣬʵ������Ҫ�õ������������ձ������������⣬����Ҫ_______________�����в�������������________________��
��ʵ������Ҫ0.1 mol��L��1��NaOH��Һ450 mL�����в���ʹ����NaOH��ҺŨ��ƫ�ߵ���__________����д��ţ���
A������ʱ���ӿ̶���
B��ѡ�õ�����ƿ������������ˮ
C������ҡ�Ⱥ�Һ���½����ּ�ˮ���̶���
D��NaOH�ܽ��δ��ȴ������ת�Ƶ�����ƿ��
(2)���Ӹֹ�ʱ���õĺ�ҩΪ�Ȼ�泥����������������Ӵ������⡣�����ķ�Ӧ��ϵ�й����������ʣ�NH4Cl��FeCl3��N2��Fe2O3��Fe��X���������⣬�ж�X�Ļ�ѧʽ��____________������������Ӧ��������___________������1mol Fe2O3�μӷ�Ӧ��ת�Ƶ��ӵ����ʵ���Ϊ________mol��
(3)200mLij��Һ����5�����Ӵ������棬����4�����ӵ����ʵ������±���
���� | H+ | K+ | NO3�� | SO42�� |
���ʵ�����mol�� | 0.5 | 0.1 | 0.6 | 0.15 |
������һ��������_______����д���ţ��������ӵ�Ũ��Ϊ_________________��
A��Fe2+ B��Cl�� C�� Al3+ D��ClO��
���𰸡���Ͳ����ͷ�ιܽ��衢����ADH2ONH4C14.5C0.5 mol��L-1
��������
(1) ��������Һһ�������������ܽ��������̣���Ҫ����Ҫ�������ձ�����Ͳ���������ͽ�ͷ�ιܵȣ�
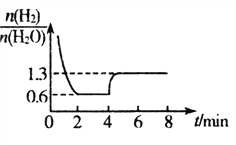
�ڸ���c=![]() ��������ʵ����ʵ���n����Һ�����V�ı仯��������������
��������ʵ����ʵ���n����Һ�����V�ı仯��������������
(2)��ҩΪ�Ȼ���������������������Ӵ����������֪����Ӧ��������Ԫ���غ�������X�������ɵ���ʱת�Ƶĵ�����������
��3����Һ���������Һ��о���ǿ�����Ե�NO3������������H+����NO3����Ӧ�����Ӳ��ܴ��������������Һ�ĵ���غ��������
(1) ��������Һһ�������������ܽ��������̣���Ҫ����Ҫ�������ձ�����Ͳ���������ͽ�ͷ�ιܵȣ������ձ������������⣬����Ҫ��Ͳ����ͷ�ι������в������������ǽ��衢������
��ˣ�������ȷ��������Ͳ����ͷ�ι������衢������
��A. ����ʱ���ӿ̶���������Һ���ƫС��Ũ��ƫ��
B.��Ϊ�����ü�ˮ����ѡ�õ�����ƿ������������ˮ��Ũ����Ӱ����
C.����ҡ�Ⱥ�Һ���½����ּ�ˮ���̶��ߣ�����Һ���ƫ��Ũ��ƫС��
D.NaOH���ձ����ܽ����δ��ȴ������ת�Ƶ�����ƿ�������ݺ���Һ���ƫС��Ũ��ƫ����
��ˣ�������ȷ������AD��
(2)���ݺ�ҩΪ�Ȼ�������������������Ӵ����������֪����Ӧ��ΪNH4Cl��Fe2O3����÷�Ӧ��������ΪFeCl3��N2��Fe��X������Ԫ���غ����֪��X�к���H��OԪ��,��XΪH2O����ƽ��ķ�Ӧ6NH4Cl+4 Fe2O3=6Fe+2 FeCl3+3 N2��+12 H2O ����NԪ�ػ��ϼ���������������FeԪ�ػ��ϼ۽�������+3�۽��͵�0��������ԭ��Fe2O3Ϊ���������ɷ���ʽ����֪������4mol Fe2O3�μӷ�Ӧʱ����18mol����ת�ƣ�����1mol Fe2O3�μӷ�Ӧ��ת�Ƶ��ӵ����ʵ���Ϊ![]() mol=4.5mol��
mol=4.5mol��
��ˣ�������ȷ������H2O��NH4C1��4.5��
��3������n(H+)+n(K+)=0.6mol��n(NO3��)+2n(SO42��)=0.9mol������Һ����غ����֪������Һ�л�Ӧ��������������Ϊ��Һ�д���H+��NO3��������ǿ����������һ��������Fe2+��Ӧ����Al3+�����ɵ���غ����֪�����ʵ���Ϊ![]() =0.1mol��c(Al3+)=
=0.1mol��c(Al3+)=![]() =0.5mol/L��
=0.5mol/L��
��ˣ�������ȷ������C ��0.5 mol��L-1��

 ��������һ���þ�ϵ�д�
��������һ���þ�ϵ�д� Сѧ��10����Ӧ����ϵ�д�
Сѧ��10����Ӧ����ϵ�д�