题目内容
【题目】某有机物A的结构简式是: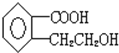 它可以通过不同的反应得到下列物质:
它可以通过不同的反应得到下列物质:
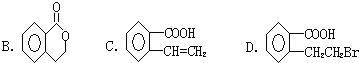
![]() 则1mol的该有机物跟足量的金属钠反应可以产生 ______
则1mol的该有机物跟足量的金属钠反应可以产生 ______ ![]() ,1mol该有机物可以跟 ______
,1mol该有机物可以跟 ______ ![]() 反应,1mol该有机物可以跟 ______ molNaOH反应。
反应,1mol该有机物可以跟 ______ molNaOH反应。
![]() 中官能团的名称是: ______ 。
中官能团的名称是: ______ 。
![]() 写出C在一定条件下反应,生成高分子化合物的化学方程式及反应类型: ______ , ______ 。
写出C在一定条件下反应,生成高分子化合物的化学方程式及反应类型: ______ , ______ 。
【答案】1 1 1 羟基、羧基 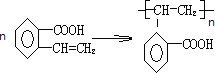 加聚反应
加聚反应
【解析】
![]()
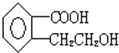 中含有1mol羧基、1mol羟基,能够与2mol钠反应生成1mol氢气,与1mol碳酸氢钠反应,与1mol氢氧化钠反应;
中含有1mol羧基、1mol羟基,能够与2mol钠反应生成1mol氢气,与1mol碳酸氢钠反应,与1mol氢氧化钠反应;
![]() 根据结构简式
根据结构简式 判断其分子中中含有的官能团名称;
判断其分子中中含有的官能团名称;
![]() 含有碳碳双键,可发生加聚反应生成高分子化合物。
含有碳碳双键,可发生加聚反应生成高分子化合物。
![]()
 中含有1mol羧基、1mol羟基,能够与2mol钠反应生成1mol氢气;只有羧基与碳酸氢钠反应,则1mol该有机物能够与1mol碳酸氢钠反应;1mol羧基能够与1mol氢氧化钠反应,
中含有1mol羧基、1mol羟基,能够与2mol钠反应生成1mol氢气;只有羧基与碳酸氢钠反应,则1mol该有机物能够与1mol碳酸氢钠反应;1mol羧基能够与1mol氢氧化钠反应,
故答案为:1;1;1;
![]()
 中含有的官能团名称为羟基和羧基,
中含有的官能团名称为羟基和羧基,
故答案为:羟基、羧基;
![]() 含有碳碳双键,可发生加聚反应生成高分子化合物,方程式为
含有碳碳双键,可发生加聚反应生成高分子化合物,方程式为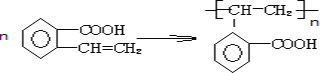 ,
,
故答案为: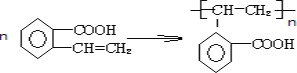 ;加聚反应。
;加聚反应。

【题目】已知:4CO(g)+2NO2(g)4CO2(g)+N2(g) ΔH=-1200 kJ·mol1。在2 L恒容密闭容器中,按照下表中甲、乙两种方式进行投料,经过一段时间后达到平衡状态,测得甲中CO的转化率为50%。下列说法中正确的是
甲 | 乙 |
0.2 mol NO2 | 0.1 mol NO2 |
0.4 mol CO | 0.2 mol CO |
A.放热反应,一定能自发进行
B.该温度下,反应的平衡常数为5
C.达平衡时,NO2的浓度:甲>乙
D.达平衡时,N2的体积分数:甲<乙
【题目】某小组同学探究Cu和H2O2的反应。
(猜想预测)
猜想1:Cu与H2O2不发生反应;
猜想2:Cu与H2O2可能发生氧化还原反应,H2O2作氧化剂。
(实验探究)
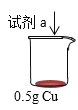
实验ⅰ:向装有0.5 g Cu的烧杯中加入20 mL 30% H2O2溶液,一段时间内无明显现象,10 小时后,溶液中有少量蓝色浑浊,Cu片表面附着少量蓝色固体。
(1)通过该实验证明了猜想2成立,写出该反应的化学方程式:________。
(继续探究)
针对该反应速率较慢,小组同学查阅资料,设计并完成了下列实验。
资料:Cu2+ + 4NH3 [ Cu(NH3)4] 2+ ,[ Cu(NH3)4] 2+为深蓝色;Cu(OH)2可溶于氨水形成深蓝色溶液。
装置 | 序号 | 试剂a | 现象 |
| ⅱ | 20 mL 30% H2O与4 mL 5 mol/L H2SO4 混合液 | Cu表面很快生产少量气泡,溶液逐渐变蓝,产生较多气泡 |
ⅲ | 20 mL 30% H2O2与4 mL5 mol/L氨水混合液 | 溶液立即变为深蓝色,产生大量气泡,Cu表面有少量蓝色不溶物 |
(2)实验ⅱ中:溶液变蓝的原因是________(用化学用语解释);经检验产生的气体为氧气,产生氧气的原因是________。
(3)对比实验ⅰ和ⅲ,为探究氨水对Cu的还原性或H2O2氧化性的影响,该同学利用如图装置继续实验。
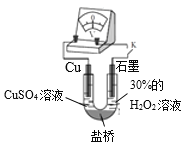
已知:电压大小反映了物质氧化还原性强弱的差异;物质氧化性与还原性强弱差异越大,电压越大。
a.K闭合时,电压为x。
b.向U型管右侧溶液中滴加氨水后,电压不变。
c.继续向U型管左侧溶液中滴加氨水后,电压增大了y。
该实验的结论:_________。利用该方法也可证明酸性增强可提高H2O2的氧化性,导致Cu溶解速率加快。
(4)对比实验ⅱ和ⅲ,实验ⅲ中产生氧气速率明显更快,可能的原因是_______。
(5)实验ⅲ有少量蓝色不溶物,小组同学加入少量NH4Cl可使其溶解,结合文字和化学用语解释不溶物溶解的原因:________。
(6)基于以上实验,影响Cu与H2O2反应速率的因素有________。
【题目】下表是几种弱酸常温下的电离平衡常数:
CH3COOH | H2CO3 | H2S | H3PO4 |
1.8×10-5 | K1=4.3×10-7 K2=5.6×10-11 | K1=9.1×10-8 K2=1.1×10-12 | K1=7.5×10-3 K2=6.2×10-8 K3=2.2×10-13 |
则下列说法中不正确的是( )
A. 碳酸的酸性强于氢硫酸
B. 多元弱酸的酸性主要由第一步电离决定
C. 常温下,加水稀释醋酸,![]() 增大
增大
D. 向弱酸溶液中加少量NaOH溶液,电离常数不变