题目内容
18.下列变化需要加人适当的氧化剂才能完成的是( )| A. | S2-→HS- | B. | FeCl2→FeCl3 | C. | H2SO4→SO2 | D. | HNO3→N2O |
分析 加入适当的氧化剂才能完成,物质变化前后,所含元素的化合价应升高,以此解答该题.
解答 解:A.S元素化合价没有发生不含,不是氧化还原反应,故A错误;
B.Fe元素化合价升高,被氧化,应加入氧化剂才能实现,故B正确;
C.S元素化合价降低,被还原,应加入还原剂才能实现,故C错误;
D.N元素化合价降低,被还原,应加入还原剂才能实现,故D错误.
故选B.
点评 本题考查氧化还原反应,为高频考点,题目难度不大,注意把握元素化合价的变化特点以及常见物质的性质,学习中注意积累.

练习册系列答案
 课堂小作业系列答案
课堂小作业系列答案 黄冈小状元口算速算练习册系列答案
黄冈小状元口算速算练习册系列答案 成功训练计划系列答案
成功训练计划系列答案 倍速训练法直通中考考点系列答案
倍速训练法直通中考考点系列答案 一卷搞定系列答案
一卷搞定系列答案 名校作业本系列答案
名校作业本系列答案
相关题目
8.下列做法正确的是( )
| A. | 用量筒量取20.21mL质量分数为98%的浓H2SO4 | |
| B. | 将5.85g NaCl溶入100mL水中,制得1 mol/LNaCl溶液 | |
| C. | 将22.4LHCl气体溶于水配成1 L且浓度为1 mol/L的盐酸 | |
| D. | 将1体积cmol/L的硫酸用水稀释为5体积,以获得浓度为0.2cmol/L的硫酸 |
9.为了探究FeS04和Cu(N03)2的混合物中各组分的含量,现设计如下流程.
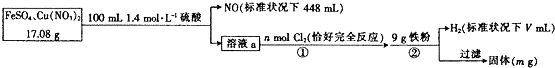
下列叙述中错误的是( )

下列叙述中错误的是( )
| A. | n=0.02 | |
| B. | y=2240 | |
| C. | 原混合物中FeS04的质量分数约为89% | |
| D. | m=3.2 |
13.强电解质和弱电解质的本质区别在于( )
| A. | 相同浓度时,溶液的导电能力的强弱 | |
| B. | 在水溶液里电解质是否全部电离为离子 | |
| C. | 是离子化合物还是共价化合物 | |
| D. | 强电解质易溶于水,弱电解质难溶于水 |
3.某原电池由M、N两根电极导线和电解质溶液组成,工作时,M电极变粗,N电极变细,由此判断该电池中电极材料和电解质溶液可能是( )
| M电极 | N电极 | 电解质溶液 | |
| A | 锌 | 铜 | 稀硫酸 |
| B | 铜 | 铁 | 稀盐酸 |
| C | 银 | 锌 | 硝酸银溶液 |
| D | 锌 | 铁 | 硝酸铁溶液 |
| A. | A | B. | B | C. | C | D. | D |
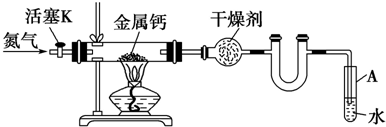
 ⑩
⑩ ⑪${\;}_{17}^{35}$Cl⑫
⑪${\;}_{17}^{35}$Cl⑫