题目内容
【题目】按照要求回答下列问题:
(1)基态 Cr 原子的价电子排布式为_______,占据最高能层的电子的电子云轮廓图形状为__。
(2)在BF3分子中,硼原子的杂化轨道类型为________,BF3和过量NaF作用可生成NaBF4,BF![]() 的立体构型为________,写出BF
的立体构型为________,写出BF![]() 的一种等电子体_______。
的一种等电子体_______。
(3)Fe3+比 Fe2+更稳定的原因是_______________________________。
(4)金刚石晶胞中面心和顶点碳原子替换成硅原子即为金刚砂晶胞,其晶胞如图所示:
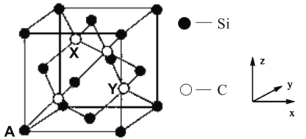
①金刚砂的化学式为_________。
②原子坐标参数表示晶胞内部各原子的相对位置。图中 A 原子坐标(0,0,0),则金刚砂晶胞中碳原子 X 的原子坐标为____________。
【答案】3d54s1 球形 sp2 正四面体 CF4(或SiF4 、CCl4等) Fe3+的价电子构型为3d5, Fe2+的价电子构型为3d6, 前者为半满状态,所以Fe3+更稳定。 SiC (![]() ,
,![]() ,
,![]() )
)
【解析】
(1)基态 Cr 原子为24号元素,价电子排布式为3d54s1;占据最高能层的电子的能级为4s,s轨道为球形,所以最高能层的电子的电子云轮廓图形状为球形;
(2)在BF3分子中,硼原子的孤电子对数为![]() ,杂化轨道数为3+0=3,所以杂化轨道类型为sp2; BF
,杂化轨道数为3+0=3,所以杂化轨道类型为sp2; BF![]() 中,硼原子的孤电子对数为
中,硼原子的孤电子对数为![]() ,价层电子对数为4+0=4,立体构型为正四面体; BF
,价层电子对数为4+0=4,立体构型为正四面体; BF![]() 的等电子体利用原子替换可以为CF4(或SiF4 、CCl4等);
的等电子体利用原子替换可以为CF4(或SiF4 、CCl4等);
(3) Fe3+的价电子构型为3d5,为半满状态较稳定,Fe2+的价电子构型为3d6,易失去一个电子为半充满稳定结构,所以Fe3+比Fe2+更稳定的原因是Fe3+的价电子构型为3d5, Fe2+的价电子构型为3d6, 前者为半满状态,所以Fe3+更稳定;
(4) ①晶胞中C原子在体心,Si原子在顶点和面心,根据均摊法得,C原子数目为4、Si原子数目为![]() ,所以金刚砂的化学式为SiC;
,所以金刚砂的化学式为SiC;
②把整个立方体分成8个相等的小立方体,X点在上层左后方的小立方体的体心,所以X 的原子坐标为(![]() ,
,![]() ,
,![]() )。
)。

 阅读快车系列答案
阅读快车系列答案