题目内容
将6mol A气体和2mol B气体在2L密闭容器中混合并在一定条件下发生反应:3A(g)+B(g)?xC(g)+2D(g).若经5min后反应达到平衡状态,容器内的压强变小,并知D的平均反应速率为0.2mol/(L?min),请填写下列空白:
①x的数值为 ;
②A的平均反应速率为 ;
③5min时B的转化率为 .
①x的数值为
②A的平均反应速率为
③5min时B的转化率为
考点:化学平衡的计算
专题:化学平衡专题
分析:达到平衡时,容器内的压强变小,所以x=1,根据三段式解题法,求出A的反应速率、B的转化率,A的反应速率=
,B的转化率为
×100%.
| △c |
| △t |
| 已转化的反应物浓度 |
| 反应物原始浓度 |
解答:
解:①达到平衡时,容器内的压强变小,所以x+2<3+1,且x为整数,所以=1,故答案为:1;
平衡时,生成的D的物质的量为 0.2mol/(L﹒min)×5min×2L=2mol,
根据三段式解题法,
3A(气)+B(气) C(气)+2D(气),
C(气)+2D(气),
开始(mol):6 2 0 0
变化(mol):3 1 1 2
平衡(mol):3 1 1 2
②A的平均反应速率为
=0.3mol/(L﹒min),故答案为:0.3mol/(L﹒min);
③B的转化率为
×100%=50%,故答案为:50%;
平衡时,生成的D的物质的量为 0.2mol/(L﹒min)×5min×2L=2mol,
根据三段式解题法,
3A(气)+B(气)
 C(气)+2D(气),
C(气)+2D(气),开始(mol):6 2 0 0
变化(mol):3 1 1 2
平衡(mol):3 1 1 2
②A的平均反应速率为
| ||
| 5min |
③B的转化率为
| 1 |
| 2 |
点评:考查化学平衡的有关计算,难度不大,关键确定x的值,注意基础知识的掌握.

练习册系列答案
相关题目
反应H2(g)+I2(g)?2HI(g)在体积固定的密闭容器中进行,达到平衡状态的标志是( )
①单位时间内断裂n mol H-H键的同时形成2n mol H-I键
②单位时间内生成n mol I2的同时生成2n mol HI
③2v正(H2)═v逆(HI)
④HI分子数不再改变
⑤混合气体颜色不再改变
⑥混合气体压强不再改变.
①单位时间内断裂n mol H-H键的同时形成2n mol H-I键
②单位时间内生成n mol I2的同时生成2n mol HI
③2v正(H2)═v逆(HI)
④HI分子数不再改变
⑤混合气体颜色不再改变
⑥混合气体压强不再改变.
| A、②④⑤⑥ | B、②③④⑤ |
| C、①③④⑤ | D、全部 |
核磁共振(NMR)技术已广泛应用于复杂分子结构的测定和医学诊断等高科技领域.已知只有质子数或中子数为奇数的原子核才有NMR现象.试判断下列哪组原子均可产生NMR现象( )
| A、18O、31P、119Sn | ||||||
| B、27Al、19F、12C | ||||||
| C、14N、18O、75As | ||||||
D、
|
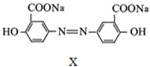 .以有机物A为原料合成X的路线如下:
.以有机物A为原料合成X的路线如下: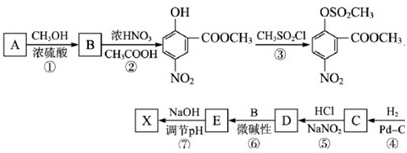
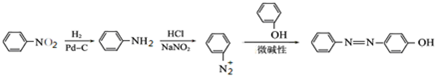
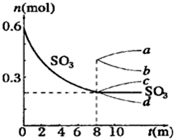 在一个2L的密闭容器中,发生反应:
在一个2L的密闭容器中,发生反应: