题目内容
反应H2(g)+I2(g)?2HI(g)在体积固定的密闭容器中进行,达到平衡状态的标志是( )
①单位时间内断裂n mol H-H键的同时形成2n mol H-I键
②单位时间内生成n mol I2的同时生成2n mol HI
③2v正(H2)═v逆(HI)
④HI分子数不再改变
⑤混合气体颜色不再改变
⑥混合气体压强不再改变.
①单位时间内断裂n mol H-H键的同时形成2n mol H-I键
②单位时间内生成n mol I2的同时生成2n mol HI
③2v正(H2)═v逆(HI)
④HI分子数不再改变
⑤混合气体颜色不再改变
⑥混合气体压强不再改变.
| A、②④⑤⑥ | B、②③④⑤ |
| C、①③④⑤ | D、全部 |
考点:化学平衡状态的判断
专题:化学平衡专题
分析:化学反应达到化学平衡状态时,正逆反应速率相等,且不等于0,各物质的浓度不再发生变化,由此衍生的一些物理量不发生变化,以此进行判断,得出正确结论.
解答:
解:①单位时间内断裂n mol H-H键的同时形成2n mol H-I键,都表示正反应速率,故不选;
②单位时间内生成n mol I2等效于消耗2n mol HI同时生成2n mol HI,正逆反应速率相等,故选;
③速率之比等于对应物质的化学计量数之比,所以2v正(H2)═v正(HI),2v正(H2)═v逆(HI),故选;
④HI分子数不再改变,物质的量不变,说明正逆反应速率相等,故选;
⑤混合气体颜色不再改变,说明碘蒸气的浓度不变,说明正逆反应速率相等,故选;
⑥混合气体压强不再改变,从反应开始到平衡一直相等,故不选;所以②③④⑤正确,故选B.
②单位时间内生成n mol I2等效于消耗2n mol HI同时生成2n mol HI,正逆反应速率相等,故选;
③速率之比等于对应物质的化学计量数之比,所以2v正(H2)═v正(HI),2v正(H2)═v逆(HI),故选;
④HI分子数不再改变,物质的量不变,说明正逆反应速率相等,故选;
⑤混合气体颜色不再改变,说明碘蒸气的浓度不变,说明正逆反应速率相等,故选;
⑥混合气体压强不再改变,从反应开始到平衡一直相等,故不选;所以②③④⑤正确,故选B.
点评:本题考查化学平衡状态的判断,题目难度不大.要注意把握平衡状态的特征.

练习册系列答案
 提分百分百检测卷单元期末测试卷系列答案
提分百分百检测卷单元期末测试卷系列答案
相关题目
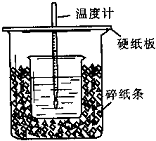 某同学用50mL 0.50mol/L的盐酸与50mL 0.55mol/L的NaOH溶液在如图所示的装置中反应,通过测定该过程中所放出的热量计算中和热.下列说法中正确的是( )
某同学用50mL 0.50mol/L的盐酸与50mL 0.55mol/L的NaOH溶液在如图所示的装置中反应,通过测定该过程中所放出的热量计算中和热.下列说法中正确的是( )| A、图中实验装置缺少环形玻璃搅拌棒 |
| B、烧杯间填满碎纸条的作用是固定小烧杯 |
| C、大小烧杯的杯口不相平,对实验结果无影响 |
| D、大烧杯上不盖硬纸板,求得的中和热△H会偏小 |
下列实验操作或对实验事实的描述正确的是( )
| A、中和热的测定实验中,可用金属丝(棒)代替环形搅拌玻璃棒 |
| B、用湿润的pH试纸测量某溶液pH时,测量值一定比真实值小 |
| C、测定硫酸铜晶体结晶水含量,若加热后的粉末表面发黑,则所测结晶水含量可能会偏高 |
| D、锌和一定量稀硫酸反应,为加快速率而不影响如的量可向溶液中加适量Cu(NO3)2晶体 |
已知428℃时,H2(g)+I2(g)?2HI(g)的平衡常数为49,则该温度下2HI(g)?H2(g)+I2(g)的平衡常数是( )
A、
| ||
B、
| ||
| C、492 | ||
| D、无法确定 |
把6molA气体和5molB气体混合放入4L密闭容器中,在一定条件下发生反应:3A(g)+B(g)?2C(g)+xD(g),经5min达到平衡,此时生成C为2mol,测定D的平均反应速率为0.1mol/(L?min),下列说法错误的是( )
| A、x=2 |
| B、B的转化率为20% |
| C、平衡时A的浓度为0.5mol/L |
| D、恒温达平衡时容器内的压强与开始时的压强相等 |
下列实验不能作为判断依据的是( )
| A、钠和钾分别与冷水反应,判断金属活动性强弱 |
| B、Br2与I2分别与足量的H2反应,判断溴与碘的非金属活动性强弱 |
| C、碳酸钠溶液显碱性,硫酸钠溶液显中性,判断硫与碳的非金属活动性强弱 |
| D、在MgSO4与Al(NO)3溶液中分别加入过量的氨水,判断镁与铝的金属活动性强弱 |
乙醇分子中不同的化学键如图所示,则乙醇在催化氧化时,化学键断裂的位置是( )


| A、②③ | B、②④ | C、①③ | D、③④ |