��Ŀ����
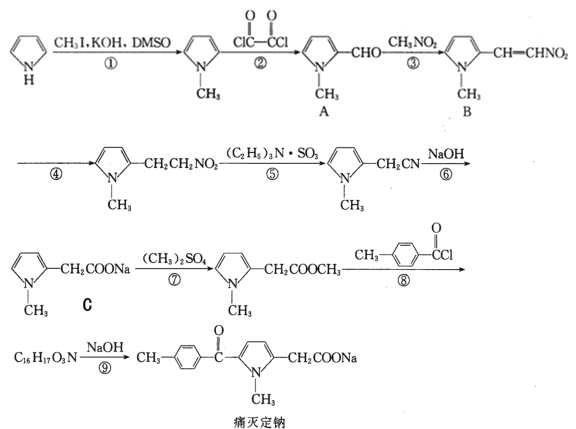
����Ŀ��ʹ������һ������������ķ����忹��ҩ����ϳ�·�����£�
�ش��������⣺
(1)������ C �к��������ŵ�������_____��
(2)��ѧ��Ӧ�ٺܵ͢ķ�Ӧ���ͷֱ�Ϊ_____��_____��
(3)���й���ʹ���Ƶ�˵����ȷ����_____��
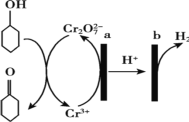
a��1mol ʹ�����������ӳ�������� 7molH2 b���˴Ź����������ܹ���ʾ 6 ���� c�����ܹ�������ԭ��Ӧ d�������ּӳɺ���������������� e����ֱ�ߵ�̼ԭ������� 4 ��
(4)��Ӧ��Ļ�ѧ����ʽΪ_____��
(5)�����廯���� X ����Է��������� A �� 14���� FeCl3 ��Һ����ɫ�Ľṹ����_____�֣������������칹�����˴Ź�����������ʾ�� 5 ����� X �Ľṹ��ʽ��_____��
(6) ���ݸ������ṩ�������Ϣ��д���ɻ�����![]() ����Ҫ���Լ��Ʊ��л�������
����Ҫ���Լ��Ʊ��л�������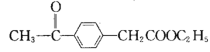 �ĺϳ�·��ͼ��________________
�ĺϳ�·��ͼ��________________
���𰸡����� ȡ����Ӧ �ӳɷ�Ӧ de  +NaOH
+NaOH ![]()
 +CH3OH 16
+CH3OH 16 ![]() ��
��![]()

��������
���ݺϳ�·��![]() ��CH3I����ȡ����Ӧ��ת��Ϊ
��CH3I����ȡ����Ӧ��ת��Ϊ![]() ��
��![]() ������Ӧ�ڣ�����λ����ȩ��ת��Ϊ��
������Ӧ�ڣ�����λ����ȩ��ת��Ϊ��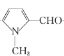 ��
��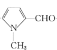 ��CH3NO2������Ӧ����
��CH3NO2������Ӧ����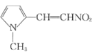 ��
��![]() �����������ӳɷ�Ӧ������
�����������ӳɷ�Ӧ������![]() ��
��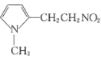 ������Ӧ�ݽ�CH2NO2��ȥ����ԭ��ת��ΪCN������
������Ӧ�ݽ�CH2NO2��ȥ����ԭ��ת��ΪCN������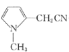 ����Ӧ����CN����ˮ��ת���COONa���õ�
����Ӧ����CN����ˮ��ת���COONa���õ�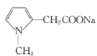 ��
��![]() ��Ӧ����
��Ӧ����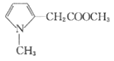 ����Ϸ���ʽC16H17O3N��
����Ϸ���ʽC16H17O3N��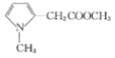 ��
��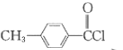 ����ȡ����Ӧ����
����ȡ����Ӧ���� ��
��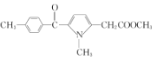 �ڼ���������ˮ��õ�
�ڼ���������ˮ��õ�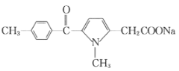 ���ݴ�����
���ݴ�����
(1)������C�к���������Ϊ�������ʴ�Ϊ��������
(2)������������֪��Ӧ��Ϊȡ����Ӧ����Ӧ��Ϊ�ӳɷ�Ӧ���ʴ�Ϊ��ȡ����Ӧ���ӳɷ�Ӧ��
(3)
b. �ýṹ����7���⣬�ʺ˴Ź����������ܹ���ʾ7���壬�ʴ���
c. ������̼̼˫�����ʻ��������������ӳɣ������������ļӳɷ�ӦҲ���ڻ�ԭ��Ӧ���ʴ���
d. �����ּӳɺ�̼̼˫����ʧ����������ԭ�ӣ��ʹ��������������䣬����ȷ��
e. ��ͼ��ʾ����ֱ�ߵ�̼ԭ������� 4 ����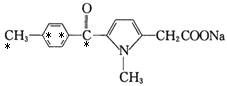 ������ȷ���ʴ�Ϊ��de��
������ȷ���ʴ�Ϊ��de��
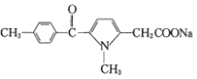
(4)�����Ϸ���֪����Ӧ��Ϊ �ڼ���������ˮ��õ�
�ڼ���������ˮ��õ� ��������Ӧ�Ļ�ѧ����ʽΪ��
��������Ӧ�Ļ�ѧ����ʽΪ�� +NaOH
+NaOH ![]()
 +CH3OH���ʴ�Ϊ��
+CH3OH���ʴ�Ϊ�� +NaOH
+NaOH ![]()
 +CH3OH��
+CH3OH��
(5)�����廯����˵��X���б�������Է���������A��14��˵����A��һ��CH2����A�IJ����Ͷ���ͬΪ4����FeCl3��Һ����ɫ˵�����з��ǻ�����������������ȡ��������Ϊ![]() (�ڡ��䡢��3��)��
(�ڡ��䡢��3��)��![]() (�ڡ��䡢��3��)����������������ȡ��������ȷ������ȡ������λ�ã����ڡ��䡢�ԣ���ȷ����һ��ȡ������λ�ã����ǻ��Ͱ���λ����λ
(�ڡ��䡢��3��)����������������ȡ��������ȷ������ȡ������λ�ã����ڡ��䡢�ԣ���ȷ����һ��ȡ������λ�ã����ǻ��Ͱ���λ����λ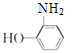 ʱ����������4����ԭ�ӣ����������4��ȡ����ʽ�����õ�4��ͬ���칹�壬ͬ�������ǻ��Ͱ���λ�ڼ�λ
ʱ����������4����ԭ�ӣ����������4��ȡ����ʽ�����õ�4��ͬ���칹�壬ͬ�������ǻ��Ͱ���λ�ڼ�λ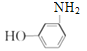 ʱ��Ҳ����4��ͬ���칹�壬���ǻ��Ͱ���λ�ڶ�λ
ʱ��Ҳ����4��ͬ���칹�壬���ǻ��Ͱ���λ�ڶ�λ![]() ʱ����2��ͬ���칹�壬��3+3+4+4+2=16�����к˴Ź�����������ʾ��5 ����� X �Ľṹ��ʽ��
ʱ����2��ͬ���칹�壬��3+3+4+4+2=16�����к˴Ź�����������ʾ��5 ����� X �Ľṹ��ʽ��![]() ��
��![]() ���ʴ�Ϊ��16��
���ʴ�Ϊ��16��![]() ��
��![]() ��
��
(6)��ȫ��������п�ͼ�з�Ӧ�ޢߢ࣬ѡ������Լ�������ɣ�![]() ����������ˮ��õ��������ƣ�����������(CH3CH2)2SO4��Ӧ�õ�
����������ˮ��õ��������ƣ�����������(CH3CH2)2SO4��Ӧ�õ�![]() ��
��![]() ���������ȷ�Ӧ����
���������ȷ�Ӧ����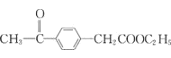 ���ϳ�·��Ϊ��
���ϳ�·��Ϊ�� ���ʴ�Ϊ��
���ʴ�Ϊ�� ��
��

����Ŀ���������л��ϳ��г��õ��ܼ���ijʵ��С����ʵ���������Ҵ���ˮ�Ʊ����ѣ� װ��ʾ��ͼ�� �гֺͼ���װ������ȥ�����й����ݺ�ʵ�鲽�裻

���� | ��Է������� | �ܶȣ�g/mL�� | �е㣨�棩 | ��ˮ�е��ܽ��� |
�Ҵ� | 46 | 0.816 | 78 | ���� |
���� | 74 | 0.713 | 34.6 | ���� |
��֪������ͬ�����£������ڱ���ʳ��ˮ�б���ˮ�и����ܡ�
���Ȼ��ƿ����Ҵ��γ������ CaCl26C2H5OH.
��ش��������⣺
��1�����Ҵ��Ʊ����ѵ��ܷ�ӦΪ2CH3CH2OH![]() CH3CH2OCH2CH3 + H2O . �˷�Ӧ���������У���һ����Ӧ�Ļ�ѧ����ʽ : CH3CH2OH +H2SO4
CH3CH2OCH2CH3 + H2O . �˷�Ӧ���������У���һ����Ӧ�Ļ�ѧ����ʽ : CH3CH2OH +H2SO4 ![]() CH3CH2OSO2OH + H2O ,��ڶ�����Ӧ�Ļ�ѧ����ʽΪ _____________________________��
CH3CH2OSO2OH + H2O ,��ڶ�����Ӧ�Ļ�ѧ����ʽΪ _____________________________��
��2������ D ��ʢ�б�ˮ����� ��������Ϊ_____________________________��
��3������1 ������Ϊ ________������2 ������Ϊ ___________��
��4����ʡ�Բ��� II�ᵼ�µĺ����_________________________________��
��5����ʵ������м���18mL �Ҵ������յõ� 8.7g ���ѣ������ѵIJ���Ϊ_____ ����������ȷ��0.1%).
����Ŀ��һ���¶��£���1.0L���ܱ������м���0.60molX��g����������ӦX(g)![]() Y(s)+2Z(g)����÷�Ӧ��X��Ũ���뷴Ӧʱ��Ĺ�ϵ�����ʾ��
Y(s)+2Z(g)����÷�Ӧ��X��Ũ���뷴Ӧʱ��Ĺ�ϵ�����ʾ��
��Ӧʱ��t/min | 0 | 1 | 2 | 3 | 4 | 6 | 8 |
c(X)/(mol��L-1) | 0.60 | 0.42 | 0.30 | 0.21 | 0.15 | a | 0.0375 |
(1)0��3min����Z��ʾ��ƽ����Ӧ�ٶ�v(Z)=___��
(2)�����÷�Ӧ�з�Ӧ���Ũ����ʱ��Ĺ�ϵ���ó��Ľ�����___���ɴ˹����Ƴ���6minʱ��Ӧ��X��Ũ��Ϊ___mol��L-1��
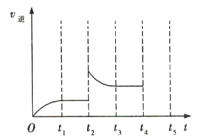
(3)�÷�Ӧ���淴Ӧ������ʱ��仯��������ͼ��ʾ��t2ʱ�ı������������___��___��
����Ŀ��һ���¶��£���1.0L���ܱ������м���0.60molX��g����������ӦX(g)![]() Y(s)+2Z(g)����÷�Ӧ��X��Ũ���뷴Ӧʱ��Ĺ�ϵ�����ʾ��
Y(s)+2Z(g)����÷�Ӧ��X��Ũ���뷴Ӧʱ��Ĺ�ϵ�����ʾ��
��Ӧʱ��t/min | 0 | 1 | 2 | 3 | 4 | 6 | 8 |
c(X)/(mol��L-1) | 0.60 | 0.42 | 0.30 | 0.21 | 0.15 | a | 0.0375 |
(1)0��3min����Z��ʾ��ƽ����Ӧ�ٶ�v(Z)=___��
(2)�����÷�Ӧ�з�Ӧ���Ũ����ʱ��Ĺ�ϵ���ó��Ľ�����___���ɴ˹����Ƴ���6minʱ��Ӧ��X��Ũ��Ϊ___mol��L-1��
(3)�÷�Ӧ���淴Ӧ������ʱ��仯��������ͼ��ʾ��t2ʱ�ı������������___��___��