题目内容
9.对水煤气的转化反应:CO(g)+H2O(g)?CO2(g)+H2(g),下列叙述正确的是( )| A. | 一定条件下,混合气体的平均相对分子质量不再改变,表明已达平衡状态 | |
| B. | 一定条件下,H2O的生成速率与CO的生成速率相等,表明已达到平衡状态 | |
| C. | 增加水蒸气浓度可提高CO的转化率 | |
| D. | 增加CO的浓度可提高CO的转化率 |
分析 该反应是反应前后气体体积不变的可逆反应,当正逆反应速率相等,各组分浓度不变时,反应达到平衡状态,增大一种反应物浓度,另一种反应物转化率增大,本身转化率减小,据此分析.
解答 解:A、混合气体的平均相对分子质量=$\frac{混合气体的质量总和}{混合气体的物质的量总和}$,混合气体的质量和物质的量不变,所以平均相对分子质量始终不变,故A错误;
B、H2O的生成速率与CO的生成速率相等,只能够说明反应速率之比等于化学计量数之比,不能说明正逆反应速率相等,故B错误;
C、增大水蒸气的浓度,平衡正向移动,CO转化率增大,故C正确;
D、增大CO浓度,CO的转化率减小,故D错误;
故选C.
点评 本题考查了化学平衡状态的判断、转化率判断,题目难度不大,注意根据正逆反应速率相等和各组分浓度不变判断平衡状态.

练习册系列答案
 提分百分百检测卷系列答案
提分百分百检测卷系列答案 宝贝计划期末冲刺夺100分系列答案
宝贝计划期末冲刺夺100分系列答案 能考试全能100分系列答案
能考试全能100分系列答案
相关题目
19.下列物质的变化,不能通过一步化学反应完成的是( )
| A. | CO2→H2CO3 | B. | SiO2→Na2SiO3 | C. | SiO2→H2SiO3 | D. | Na2O2→Na2CO3 |
17.X、Y、Z、W为四种短周期元素,有关这四种元素的说法中一定正确的是( )
| 元素 | X | Y | Z | W |
| 原子半径(nm) | 0.077 | 0.075 | 0.102 | 0.099 |
| 最高正价或最低负价 | +4 | +5 | -2 | -1 |
| A. | 1mol W的单质参加氧化还原反应时转移的电子数为2mol | |
| B. | X与W形成XW4时,各原子最外层均满足8电子稳定结构 | |
| C. | 0.3mol Cu分别与足量HYO3和H2ZO4的稀溶液反应均产生0.2mol气体 | |
| D. | Y的氢化物与W的氢化物反应的产物只含有共价键 |
4.某有机物的结构简式为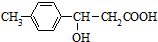 ,它可发生的有机反应的正确组合是( )
,它可发生的有机反应的正确组合是( )
①取代 ②加成 ③消去 ④水解 ⑤酯化 ⑥中和 ⑦氧化 ⑧加聚.
 ,它可发生的有机反应的正确组合是( )
,它可发生的有机反应的正确组合是( )①取代 ②加成 ③消去 ④水解 ⑤酯化 ⑥中和 ⑦氧化 ⑧加聚.
| A. | ①②③⑤⑥ | B. | ②③④⑥⑧ | C. | ①②③⑤⑥⑦ | D. | ④⑤⑥⑦⑧ |
1.下列解释实验事实的离子方程式不正确的是( )
| A. | 用烧碱溶液吸收NO2:2NO2+2OH-=NO3-+NO2-+H2O | |
| B. | 用烧碱溶液吸收氯气:Cl2+2OH-=Cl-+ClO-+H2O | |
| C. | 明矾溶液与过量氨水反应:Al3++3NH3.H2O=Al(OH)3↓+3NH4+ | |
| D. | 酸性KI淀粉溶液久置后变蓝:4I-+O2+2H2O=2I2+4OH- |
10.天然纤维是自然界原有的或经人工培植的植物上、人工饲养的动物上直接取得的纺织纤维.化学纤维指用天然的或合成的聚合物为原料,经化学方法制成的纤维.下列物质属于天然纤维且其主要成份是纤维素的是( )
| A. | 光导纤维 | B. | 人造丝 | C. | 棉花 | D. | 蚕丝 |
11.短周期元素W、X、Y、Z在元素周期表中的相对位置如表所示,这四种元素的元素的原子最外层电子数之和为20.则下列说法不正确的是( )
| X | Y | |||
| W | Z |
| A. | 最高价氧化物的水化物的酸性:X<Z | |
| B. | 原子半径大小:Y<W | |
| C. | 工业上用电解熔融的W与Z所形成的化合物来制取W | |
| D. | W和Y形成的化合物可与Z的氢化物的水溶液发生反应 |

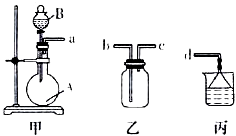 熟悉和使用中学化学实验中常见仪器及用品,是化学学习的基本要求.试回答以下问题:
熟悉和使用中学化学实验中常见仪器及用品,是化学学习的基本要求.试回答以下问题: