题目内容
下列关于阿伏伽德罗常数的叙述,错误的是( )
| A、1L 1mol/L的次氯酸钠溶液中含有次氯酸根离子的数目为NA |
| B、1mol氯气和足量NaOH溶液反应转移的电子书为2NA |
| C、10L 0.1mol/L的碳酸钠溶液中,钠离子、碳酸根离子的总数为3NA |
| D、在含4mol Si-O键的二氧化硅晶体中,氧原子的数目为4NA |
考点:阿伏加德罗常数
专题:阿伏加德罗常数和阿伏加德罗定律
分析:A.次氯酸为弱电解质,次氯酸根离子在溶液中部分发生水解,导致次氯酸根离子数目减少;
B.氯气与氢氧化钠溶液的反应中,氯气既是氧化剂也是还原剂,1mol氯气完全反应转移了1mol电子;
C.碳酸钠溶液中,碳酸根离子部分水解,导致溶液中碳酸根离子数目减少;
D.1mol二氧化硅中含有4mol硅氧键,据此判断二氧化硅的物质的量及含有的氧原子数目.
B.氯气与氢氧化钠溶液的反应中,氯气既是氧化剂也是还原剂,1mol氯气完全反应转移了1mol电子;
C.碳酸钠溶液中,碳酸根离子部分水解,导致溶液中碳酸根离子数目减少;
D.1mol二氧化硅中含有4mol硅氧键,据此判断二氧化硅的物质的量及含有的氧原子数目.
解答:
解:A. 1L 1mol/L的次氯酸钠溶液中含有次氯酸钠1mol,由于次氯酸根离子部分水解,则溶液中次氯酸根离子小于1mol,溶液中含有次氯酸根离子的数目小于NA,故A错误;
B.1mol 氯气和足量NaOH溶液反应转移了1mol导致,转移的电子数为NA,故B错误;
C.10L 0.1mol/L的碳酸钠溶液中含有溶质碳酸钠1mol,由于碳酸根离子部分水解,溶液中碳酸根离子需要1mol,所以溶液中钠离子、碳酸根离子总物质的量小于3mol,钠离子、碳酸根离子的总数小于3NA,故C错误;
D.含4mol Si-O键的二氧化硅晶体中含有1mol二氧化硅,含有2mol氧原子,含有的氧原子的数目为2NA,故D错误;
故选ABCD.
B.1mol 氯气和足量NaOH溶液反应转移了1mol导致,转移的电子数为NA,故B错误;
C.10L 0.1mol/L的碳酸钠溶液中含有溶质碳酸钠1mol,由于碳酸根离子部分水解,溶液中碳酸根离子需要1mol,所以溶液中钠离子、碳酸根离子总物质的量小于3mol,钠离子、碳酸根离子的总数小于3NA,故C错误;
D.含4mol Si-O键的二氧化硅晶体中含有1mol二氧化硅,含有2mol氧原子,含有的氧原子的数目为2NA,故D错误;
故选ABCD.
点评:本题考查阿伏加德罗常数的有关计算和判断,题目难度中等,试题侧重考查盐的水解原理,注意掌握好以物质的量为中心的各化学量与阿伏加德罗常数的关系,选项D为易错点,注意明确二氧化硅晶体中,1mol二氧化硅中含有4mol硅氧键.

练习册系列答案
 阅读快车系列答案
阅读快车系列答案
相关题目
下列现象或事实可用同一原理解释的是( )
| A、浓硫酸和浓盐酸长期暴露在空气中浓度均降低 |
| B、氯水和双氧水均要盛装在棕色试剂瓶中 |
| C、SO2能使品红溶液和溴水均褪色 |
| D、NaCl固体中混有NH4Cl或I2,均可用加热法除去 |
有关糖类的叙述中,正确的一项是( )
| A、糖类是具有甜味的物质 |
| B、糖类是具有Cn(H2O)m通式的物质 |
| C、糖类是含有醛基的物质 |
| D、糖类一般是多羟基醛或多羟基酮以及能水解产生它们的物质 |
下列四组溶液,不用其他试剂就能鉴别开来的是( )
①AgNO3溶液、稀氨水
②NaAlO2、KHCO3、NaCl、NaHSO4
③HNO3、Na2SO3、Na2SO4、BaCl2
④AlCl3、NaAlO2.
①AgNO3溶液、稀氨水
②NaAlO2、KHCO3、NaCl、NaHSO4
③HNO3、Na2SO3、Na2SO4、BaCl2
④AlCl3、NaAlO2.
| A、① | B、①②④ | C、①②③ | D、全部 |
有关盐类水解的说法不正确的是( )
| A、盐类的水解过程促进了水的电离平衡 |
| B、盐类的水解是中和反应的逆反应 |
| C、盐类的水解结果使盐溶液不一定呈中性 |
| D、Na2CO3溶液中,Na+的浓度是CO32-浓度的2倍 |
燃烧下列混合气体,所产生的CO2的量一定小于燃烧相同质量的丙烯所产生的CO2的是( )
| A、丁烯、丙烯 |
| B、乙炔、乙烯 |
| C、乙炔、丙烷 |
| D、乙烯、丙烷 |
下列有机物的命名,正确的是( )
| A、2,3,3,8,8-五甲基壬烷 |
| B、2,2,7,7,8-五甲基壬烷 |
| C、2,3,3,5,5-五甲基戊烷 |
| D、2,2,4,4,5-五甲基戊烷 |
关于下列各实验装置的叙述中,不正确的是( )
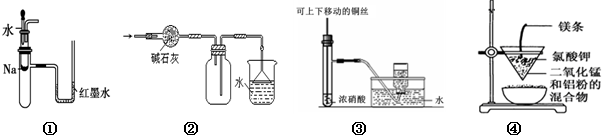

| A、装置①可用于验证Na与H2O反应是否放热 |
| B、装置②可用于干燥、收集NH3,并吸收多余的NH3 |
| C、装置③可用于制备并收集少量NO2 |
| D、装置④可制得金属锰 |