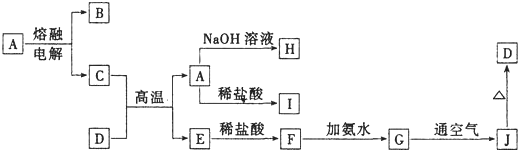
题目内容
有关盐类水解的说法不正确的是( )
| A、盐类的水解过程促进了水的电离平衡 |
| B、盐类的水解是中和反应的逆反应 |
| C、盐类的水解结果使盐溶液不一定呈中性 |
| D、Na2CO3溶液中,Na+的浓度是CO32-浓度的2倍 |
考点:盐类水解的应用
专题:盐类的水解专题
分析:A.酸或碱抑制水电离,含有弱离子的盐促进水电离;
B.在溶液中,强碱弱酸盐、强酸弱碱盐或弱酸弱碱盐电离出来的离子与水电离出来的H+与OH-生成弱电解质的过程叫做盐类水解;
C.盐类的水解结果使盐溶液不一定呈中性,可能呈酸性或碱性;
D.碳酸钠溶液中,碳酸根离子水解、钠离子不水解.
B.在溶液中,强碱弱酸盐、强酸弱碱盐或弱酸弱碱盐电离出来的离子与水电离出来的H+与OH-生成弱电解质的过程叫做盐类水解;
C.盐类的水解结果使盐溶液不一定呈中性,可能呈酸性或碱性;
D.碳酸钠溶液中,碳酸根离子水解、钠离子不水解.
解答:
解:A.酸或碱抑制水电离,盐类水解是含有弱离子的盐和水反应生成弱电解质,则含有弱离子的盐促进水电离,故A正确;
B.在溶液中,强碱弱酸盐、强酸弱碱盐或弱酸弱碱盐电离出来的离子与水电离出来的H+与OH-生成弱电解质的过程叫做盐类水解,所以盐类的水解是中和反应的逆反应,故B正确;
C.盐类的水解结果使盐溶液不一定呈中性,可能呈酸性或碱性,如强酸弱碱盐溶液呈酸性、强碱弱酸盐溶液呈碱性,故C正确;
D.碳酸钠是强碱弱酸盐,碳酸钠溶液中,碳酸根离子水解、钠离子不水解,所以Na+的浓度大于CO32-浓度的2倍,故D错误;
故选D.
B.在溶液中,强碱弱酸盐、强酸弱碱盐或弱酸弱碱盐电离出来的离子与水电离出来的H+与OH-生成弱电解质的过程叫做盐类水解,所以盐类的水解是中和反应的逆反应,故B正确;
C.盐类的水解结果使盐溶液不一定呈中性,可能呈酸性或碱性,如强酸弱碱盐溶液呈酸性、强碱弱酸盐溶液呈碱性,故C正确;
D.碳酸钠是强碱弱酸盐,碳酸钠溶液中,碳酸根离子水解、钠离子不水解,所以Na+的浓度大于CO32-浓度的2倍,故D错误;
故选D.
点评:本题考查了盐类水解,明确盐类水解的含义是解本题关键,根据“谁强谁显性、谁弱谁水解、强强显中性”确定溶液酸碱性,题目难度不大.

练习册系列答案
 新课标快乐提优暑假作业陕西旅游出版社系列答案
新课标快乐提优暑假作业陕西旅游出版社系列答案 暑假衔接培优教材浙江工商大学出版社系列答案
暑假衔接培优教材浙江工商大学出版社系列答案 欣语文化快乐暑假沈阳出版社系列答案
欣语文化快乐暑假沈阳出版社系列答案
相关题目
意大利科学家使用氧分子和带正电的氧离子作用,合成出新型氧分子O4,反应过程可表示为:2O2
O4,下列说法错误的是( )
| ||
| A、O4与O2、O3都是氧的同素异形体 |
| B、合成O4属于物理变化 |
| C、O4与O2的化学性质完全相同 |
| D、O4的密度比O2大 |
下列仪器中,通常不能用作反应容器的是( )
| A、容量瓶 | B、烧杯 |
| C、锥形瓶 | D、量筒 |
氧化还原反应发生在同种元素之间的是( )
| A、Zn+2HCl═ZnCl2+H2↑ | ||||
| B、2H2S+SO2═3S+2H2O | ||||
| C、H2+CuO═Cu+H2O | ||||
D、2H2O
|
下列物质中,与葡萄糖具有不同最简式的是( )
| A、甲醛 | B、蔗糖 |
| C、甲酸甲酯 | D、果糖 |
下列关于阿伏伽德罗常数的叙述,错误的是( )
| A、1L 1mol/L的次氯酸钠溶液中含有次氯酸根离子的数目为NA |
| B、1mol氯气和足量NaOH溶液反应转移的电子书为2NA |
| C、10L 0.1mol/L的碳酸钠溶液中,钠离子、碳酸根离子的总数为3NA |
| D、在含4mol Si-O键的二氧化硅晶体中,氧原子的数目为4NA |
下面有关碳酸钠与碳酸氢钠性质的描述,不正确的是( )
| A、受热时碳酸钠比碳酸氢钠稳定 |
| B、在同温下,碳酸钠比碳酸氢钠的溶解度大 |
| C、物质的量相等的碳酸钠与碳酸氢钠分别溶于水后,碳酸氢钠水溶液的碱性较强 |
| D、相同物质的量的碳酸钠与碳酸氢钠分别与足量的盐酸反应,两者放出的二氧化碳一样多 |
药物是人们生活的必备品之一,下列四种药物都能发生取代、加成、水解、中和四种反应的是( )
A、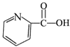 维生素 |
B、 阿司匹林 |
C、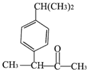 芬必得 |
D、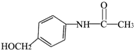 扑热息痛 扑热息痛 |