题目内容
【题目】某课外学习小组对日常生活中不可缺少的调味品M进行探究.已知C可在D中燃烧发出苍白色火焰.M与其他物质的转化关系如图1所示(部分产物已略去): 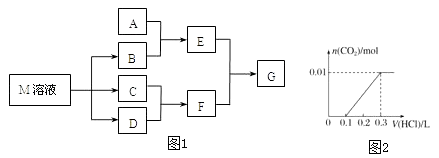
(1)写出用惰性电极电解M溶液的离子方程式 . 写出F的电子式
(2)若A是一种常见的酸性氧化物,且可用于制造玻璃,E溶液与F溶液反应可以制备一种胶体,则E溶液的俗称是 .
(3)若A是CO2气体,A与B溶液能够反应,反应后所得的溶液再与盐酸反应,如图所示:则A与B溶液反应后溶液中的溶质化学式为 .
(4)若A是一种常见金属单质,且A与B溶液能够反应,则将过量的F溶液逐滴加入E溶液,边加边振荡,所看到的实验现象是
(5)若A是一种不稳定的盐,A溶液与B溶液混合将产生白色絮状沉淀且瞬间变为灰绿色,最后变成红褐色的E,向G溶液中加入苯酚溶液后显紫色,则由A转化成E的离子方程式是 .
(6)若A是一种化肥.实验室可用A和B反应制取气体E,E与F、E与D相遇均冒白烟,且利用E与D的反应检验输送D的管道是否泄露,写出E与D反应的化学方程式是 .
(7)若A是一种溶液,只可能含有H+、NH4+、Mg2+、Fe3+、Al3+、CO32﹣、SO42﹣中的某些离子,当向该溶液中加入B溶液时发现生成沉淀的物质的量随B溶液的体积发生变化如图2所示,由此可知,该溶液中肯定含有的离子及其浓度之比为 .
【答案】
(1)2Cl﹣+2H2O ![]() 2OH﹣+H2↑+Cl2↑;
2OH﹣+H2↑+Cl2↑;![]()
(2)水玻璃
(3)Na2CO3和NaHCO3
(4)溶液中逐渐有白色絮状沉淀生成,且不断增加;然后又由多到少,最后消失
(5)4Fe2++8OH﹣+O2+2H2O=4Fe(OH)3↓
(6)3Cl2+8NH3=N2+6NH4Cl
(7)c(H+):c(Al3+):c(NH4+):c(SO42﹣)=1:1:2:3
【解析】解:(1)C可在D中燃烧发出苍白色火焰,为氢气与氯气反应生成HCl,可推知C为H2、D为Cl2、F为HCl,M是日常生活中不可缺少的调味品,由转化关系可知,M的溶液电解生成氢气、氯气与B,可推知M为NaCl、B为NaOH,用惰性电极电解M溶液的离子方程式为:2Cl﹣+2H2O ![]() 2OH﹣+H2↑+Cl2↑,HCl分子中H原子与Cl原子之间形成1对共用电子对,其电子式为:
2OH﹣+H2↑+Cl2↑,HCl分子中H原子与Cl原子之间形成1对共用电子对,其电子式为: ![]() , 所以答案是:2Cl﹣+2H2O
, 所以答案是:2Cl﹣+2H2O ![]() 2OH﹣+H2↑+Cl2↑;
2OH﹣+H2↑+Cl2↑; ![]() (2)若A是一种常见的酸性氧化物,且可用于制造玻璃,则A为SiO2 , E为Na2SiO3 , 与F溶液反应可以制备G为H2SiO3 , E的溶液俗称水玻璃,
(2)若A是一种常见的酸性氧化物,且可用于制造玻璃,则A为SiO2 , E为Na2SiO3 , 与F溶液反应可以制备G为H2SiO3 , E的溶液俗称水玻璃,
所以答案是:水玻璃;(3)若A是CO2气体,CO2与NaOH溶液能够反应生成碳酸钠或碳酸氢钠或两者的混合物,也有可能氢氧化钠过量,根据反应后所得的溶液再与盐酸反应产生气体的图2所示可知,盐酸体积为0.1L时没有气体,而用了0.2L的盐酸产生气体,碳酸钠溶液生成碳酸氢钠的用掉的盐酸与碳酸氢钠产生二氧化碳用的掉的盐酸相等,由此判断反应后溶液中的溶质为Na2CO3和NaHCO3 ,
所以答案是:Na2CO3和NaHCO3;(4)若A是一种常见金属单质,且与NaOH溶液能够反应,则A为Al,E为NaAlO2 , 则将过量的HCl溶液逐滴加入NaAlO2溶液中,先生成氢氧化铝,而后氢氧化铝溶解,故看到的现象为:溶液中逐渐有白色絮状沉淀生成,且不断地增加,随后沉淀逐渐溶解最终消失,
所以答案是:溶液中逐渐有白色絮状沉淀生成,且不断增加;然后又由多到少,最后消失;(5)若A是一种不稳定的盐,A溶液与B溶液混合将产生白色絮状沉淀且瞬间变为灰绿色,最后变成红褐色的E,可推知A中含有Fe2+ , E为Fe(OH)3 , G为FeCl3 , 则由A转化成E的离子方程式是:4Fe2++8OH﹣+O2+2H2O=4Fe(OH)3↓,
所以答案是:4Fe2++8OH﹣+O2+2H2O=4Fe(OH)3↓;(6)若A是一种化肥,实验室可用A和NaOH反应制取气体E,则E为NH3、A为铵盐,E与氯气相遇均冒白烟,且利用E与氯气的反应检验输送氯气的管道是否泄露,则氨气与氯气反应生成氯化铵,同时生成氮气,反应方程式为:3Cl2+8NH3=N2+6NH4Cl,
所以答案是:3Cl2+8NH3=N2+6NH4Cl;(7)由图可知,开始加入NaOH没有沉淀和气体产生,则一定有H+ , 一定没有CO32﹣ , 后来有沉淀产生且最后消失,则一定没有Mg2+、Fe3+ , 一定含有Al3+;中间段沉淀的质量不变,应为NH4++OH﹣=NH3H2O的反应,则含有NH4+ , 由电荷守恒可知一定含有SO42﹣ ,
发生反应H++OH﹣=H2O,氢离子消耗NaOH溶液的体积为1积,
发生反应Al3++3OH﹣=Al(OH)3↓,铝离子消耗NaOH溶液的体积为3体积,
发生反应NH4++OH﹣=NH3H2O,铵根消耗氢氧化钠为2体积,
则n(H+):n(Al3+):n(NH4+)=1:1:2,由电荷守恒可知,n(H+):n(Al3+):n(NH4+):n(SO42﹣)=1:1:2:3,故c(H+):c(Al3+):c(NH4+):c(SO42﹣)=1:1:2:3,
所以答案是:c(H+):c(Al3+):c(NH4+):c(SO42﹣)=1:1:2:3.

 智趣寒假作业云南科技出版社系列答案
智趣寒假作业云南科技出版社系列答案