题目内容
【题目】磷化铜(Cu3P2)用于制造磷青铜、磷青铜是含少量锡、磷的铜合金,主要用作耐磨零件和弹性原件.
(1)基态铜原子的电子排布式为;价电子中成对电子数有个.
(2)磷化铜与水作用产生有毒的磷化氢(PH3). ①PH3分子中的中心原子的杂化方式是 .
②P与N同主族,其最高价氧化物对应水化物的酸性:HNO3H3PO4(填“>”或“<”),从结构的角度说明理由: .
(3)磷青铜中的锡、磷两元素电负性的大小为SnP(填“>”“<”或“=”).
(4)某磷青铜晶胞结构如图所示. 
①则其化学式为 .
②该晶体中距离Cu原子最近的Sn原子有个,这些Sn原子所呈现的构型为 .
③若晶体密度为8.82g/cm3 , 最近的Cu原子核间距为pm(用含NA的代数式表示).
【答案】
(1)1s22s22p63s23p63d104s1或[Ar]3d104s1;10
(2)sp3;>;因为HNO3分子结构中含有2个非烃基氧原子,比H3PO4中多1个
(3)<
(4)SnCu3P;4;平面正方形;![]() ×
× ![]() ×1010
×1010
【解析】解:(1)Cu元素为29号元素,原子核外有29个电子,所以核外电子排布式为:1s22s22p63s23p63d104s1或[Ar]3d104s1 , 铜原子价电子3d104s1 , 其中成对电子数10个, 所以答案是:1s22s22p63s23p63d104s1或[Ar]3d104s1;10;(2)①.PH3分子中价层电子对个数=σ键个P数+孤电子对个数=3+ ![]() (5﹣3×1)=4,所以磷原子采用sp3杂化,所以答案是:sp3;②非金属性N>P,对应最高价氧化物对应的水化物的酸性为HNO3>H3PO4 , 从结构的角度因为HNO3分子结构中含有2个非烃基氧原子,比H3PO4中多1个,酸性为HNO3>H3PO4 , 所以答案是:>;因为HNO3分子结构中含有2个非烃基氧原子,比H3PO4中多1个;(3)磷青铜中的锡、磷两元素电负性的大小为Sn<P,所以答案是:<;(4)①
(5﹣3×1)=4,所以磷原子采用sp3杂化,所以答案是:sp3;②非金属性N>P,对应最高价氧化物对应的水化物的酸性为HNO3>H3PO4 , 从结构的角度因为HNO3分子结构中含有2个非烃基氧原子,比H3PO4中多1个,酸性为HNO3>H3PO4 , 所以答案是:>;因为HNO3分子结构中含有2个非烃基氧原子,比H3PO4中多1个;(3)磷青铜中的锡、磷两元素电负性的大小为Sn<P,所以答案是:<;(4)① 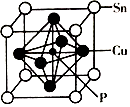 ,晶体中P原子位于中心,含有一个磷原子,立方体每个面心喊一个Cu,每个Cu分摊给一个晶胞的占
,晶体中P原子位于中心,含有一个磷原子,立方体每个面心喊一个Cu,每个Cu分摊给一个晶胞的占 ![]() ,立方体顶角Sn分摊给每个晶胞的原子为
,立方体顶角Sn分摊给每个晶胞的原子为 ![]() ,据此得到化学式SnCu3P,
,据此得到化学式SnCu3P,
所以答案是:SnCu3P;②该晶体中距离Cu原子最近的Sn原子有4个,这些Sn原子所呈现的构型为平面正方形,所以答案是:4;平面正方形;③摩尔质量=342g/mol,则一个晶胞质量 ![]() g,设立方体边长为x,铜原子间最近距离为a,则a2=(
g,设立方体边长为x,铜原子间最近距离为a,则a2=( ![]() )2+(
)2+( ![]() )2 , a=
)2 , a= ![]() x,结合密度ρ=
x,结合密度ρ= ![]() ,V=x3=
,V=x3= 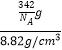 =
= ![]() cm3 , x=
cm3 , x= ![]() cm,a=
cm,a= ![]() x=
x= ![]() ×
× ![]() cm═
cm═ ![]() ×
× ![]() ×1010pm,所以答案是:
×1010pm,所以答案是: ![]() ×
× ![]() ×1010 .
×1010 .

 互动课堂系列答案
互动课堂系列答案 激活思维智能训练课时导学练系列答案
激活思维智能训练课时导学练系列答案【题目】除去下列物质中的杂质,所用试剂和方法正确的是( )
选项 | 物质 | 杂质 | 除杂质所用试剂和方法 |
A | KCl溶液 | I2 | CCl4,萃取 |
B | KNO3 | K2SO4 | BaCl2溶液,过滤 |
C | Fe | Cu | 稀硫酸,过滤 |
D | CaCO3 | CaO | 稀盐酸,过滤 |
A. A B. B C. C D. D