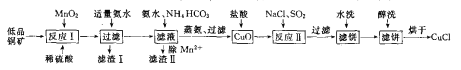
题目内容
【题目】A、B、C、D、E、F是原子序数依次增大的短周期主族元素,A的原子核内无中子,B、F在元素周期表中的相对位置 如图,B与氧元素能形成两种无色气体,D是地壳中含量最多的元素,E是地壳中含量最多的金属元素。
B | ||
F |
(1)BF2的结构式为____________。
(2)D和 F氢化物中沸点较高的___________________填化学式)。
(3)工业制取E单质的化学方程式为______________。
(4)在微电子工业中,C的最简单气态氢化物的水溶液可作刻蚀剂H2O2的清除剂,所发生反应的产物不污染环境,其化学方程式为______________。
(5)火箭使用B2A8C2作燃料,N2O4为氧化剂,燃烧放出的巨大能量能把火箭送入 太空,并且产生三种无污染的气体,其化学方程式为____________。
【答案】 S=C=S H2O 2Al2O3![]() 4Al+3O2↑ 2NH3+3H2O2=N2+6H2O C2H8N2+2N2O4=2CO2↑+3N2↑+4H2O↑ 。
4Al+3O2↑ 2NH3+3H2O2=N2+6H2O C2H8N2+2N2O4=2CO2↑+3N2↑+4H2O↑ 。
【解析】A、B、C、D、E、F是原子序数依次增大的短周期主族元素,A的原子核内无中子,A是H元素,B、F在元素周期表中的相对位置 如图,B与氧元素能形成两种无色气体CO、CO2,故B为C元素;D是地壳中含量最多的元素,D是O元素,C为N元素,E是地壳中含量最多的金属元素,E是Al元素,F为硫元素。
(1)BF2为CS2,碳和硫间形成两个共用电子对,结构式为S=C=S,(2)水分子间形成氢键,H2O比H2S的沸点高,D和 F氢化物中沸点较高的 H2O;(3)工业制取Al单质用电解Al2O3的方法,化学方程式为2Al2O3![]() 4Al+3O2↑ ;(4). 2NH3+3H2O2=N2+6H2O (5)火箭使用B2A8C2作燃料,N2O4为氧化剂,其化学方程式为C2H8N2+2N2O4=2CO2↑+3N2↑+4H2O↑
4Al+3O2↑ ;(4). 2NH3+3H2O2=N2+6H2O (5)火箭使用B2A8C2作燃料,N2O4为氧化剂,其化学方程式为C2H8N2+2N2O4=2CO2↑+3N2↑+4H2O↑

【题目】铜及其化合物在工农业生产及日常生活中应用非常广泛。回答下列问题:
(1)纳米级Cu2O由于具有优良的催化性能而受到关注,制取Cu2O的两种方法如下表所示。
方法I | 用炭粉在高温条件下还原CuO生成Cu2O和CO2 |
方法II | 用肼(N2H4)还原新制Cu(OH)2 |
① 方法I中还原剂与氧化剂的物质的量之比为________。
② 方法II发生反应的化学方程式为______________。
(2)氢化亚铜是一种红色同体,可由下列反应制备:
4CuSO4+3H3PO2+6H2O=4CuH↓+4H2SO4+3H3PO4
该反应中每转移3 mol电子,生成CuH的物质的量为___________mol。
(3)氯化铜溶液中各种含铜微粒的分布分数(平衡时某微粒的浓度占各微粒浓度之和的分数)与c(C1-)之间的关系如图所示。
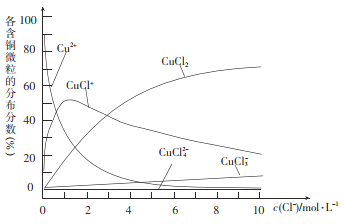
① 当c(C1-)= 9 mol/L时,溶液中3种主要含铜微粒浓度的大小关系为__________。
② 在c(C1-)= l mol /L的氯化铜溶液中,加人AgNO3溶液,CuCl+转化为Cu2+的离子方程式为____________。
(4)已知:Cu(OH)2是二元弱碱,25℃时Ksp[Cu(OH)2]=2.0×10-20。则此温度下在铜盐溶液中Cu2+发生水解反应的平衡常数为______________。