题目内容
12.已知NH4CuSO3与足量的10mol/L硫酸混合微热,产生下列现象:①有红色金属生成 ②产生刺激性气味的气体 ③溶液呈现蓝色.据此判断下列说法正确的是( )| A. | 刺激性气味的气体是氨气 | |
| B. | NH4CuSO3中硫元素被氧化 | |
| C. | 1 mol NH4CuSO3完全反应转移0.5 mol电子 | |
| D. | 反应中硫酸作氧化剂 |
分析 NH4CuSO3与硫酸混合微热,生成红色固体物、产生有刺激性气味的气体和蓝色溶液,说明反应生成Cu、SO2和Cu2+,则NH4CuSO3中Cu的化合价为+1价,以此解答该题.
解答 解:反应的发产生为:2NH4CuSO3+4H+═Cu+Cu2++2SO2↑+2H2O+2NH4+.
A、因反应是在酸性条件下进行,不可能生成氨气,故A错误;
B、NH4CuSO3与硫酸混合微热,生成红色固体物、产生有刺激性气味的气体和蓝色溶液,说明反应生成Cu、SO2和Cu2+,反应前后S元素的化合价没有发生变化,故B错误;
C、反应只有Cu元素的化合价发生变化,分别由+1→+2,+1→0,反应的发产生为:2NH4CuSO3+4H+═Cu+Cu2++2SO2↑+2H2O+2NH4+,每2molNH4CuSO3参加反应则转移1mol电子,则1molNH4CuSO3完全反应转移0.5mol电子,故C正确.
D、由发产生为:2NH4CuSO3+4H+═Cu+Cu2++2SO2↑+2H2O+2NH4+,反应只有Cu元素的化合价发生变化,硫酸根反应前后未变,反应中硫酸体现酸性,故D错误;
故选:C.
点评 本题考查氧化还原反应,难度较大,注意从反应现象判断生成物,结合化合价的变化计算电子转移的数目.

练习册系列答案
相关题目
2.下列物质的水溶液中,加入Ba(OH)2溶液后,原溶液中阴、阳离子都减少的是( )
| A. | CuSO4 | B. | Ca(NO3)2 | C. | Na2CO3 | D. | FeCl3 |
3.质谱图显示,某化合物的相对分子质量为74,燃烧实验发现其分子内碳、氢原子个数之比为2:5,核磁共振氢谱显示,该物质中只有两种类型的氢原子.关于该化合物的描述中,不正确的是( )
| A. | 该化合物可能为2甲基2丙醇 | B. | 该化合物为2丁醇的同分异构体 | ||
| C. | 该化合物可能为乙醚 | D. | 该化合物为乙醚的同系物 |
20.能源问题十分紧迫,化石燃料来源有限且终会枯竭,其燃烧产物的排放引起的温室效应让人忧心忡忡;石油价格普遍上涨;新能源的开发成为急需研究的课题.那么新的替代能源主要包括( )
①核能 ②柴草 ③煤炭 ④石油 ⑤氢能 ⑥太阳能 ⑦水煤气 ⑧天然气.
①核能 ②柴草 ③煤炭 ④石油 ⑤氢能 ⑥太阳能 ⑦水煤气 ⑧天然气.
| A. | ②③④⑦ | B. | ①⑤⑥ | C. | ②④⑦⑧ | D. | ①②⑥ |
7.如图是硫酸试剂标签上的部分内容.下列说法正确的是( )


| A. | 配制950ml 2.3mol/LH2SO4溶液需要取该硫酸125.0mL | |
| B. | 1molAl与足量该硫酸反应产生3g氢气 | |
| C. | 该硫酸在空气中露置,溶质的质量分数会逐渐减小 | |
| D. | 该硫酸不能用来干燥二氧化硫 |
17.下列各化合物的命名不正确的是( )
| A. | 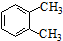 邻二甲苯 邻二甲苯 | B. | 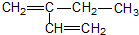 2-乙基-1,3-丁二烯 2-乙基-1,3-丁二烯 | ||
| C. | 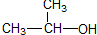 1-甲基乙醇 1-甲基乙醇 | D. | 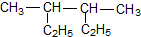 3,4-二甲基己烷 3,4-二甲基己烷 |
4.下列化合物中,含有非极性共价键的离子化合物是( )
| A. | Na2O2 | B. | H2SO4 | C. | Ba(OH)2 | D. | N2 |
1.浓硫酸有吸水性,常用作气体干燥剂,下列气体不能用浓硫酸干燥的是( )
| A. | Cl2 | B. | NH3 | C. | SO2 | D. | CH4 |
 立方烷的结构简式如图所示,每个顶点是一个碳原子.则:
立方烷的结构简式如图所示,每个顶点是一个碳原子.则: