��Ŀ����
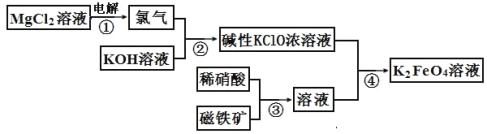
����Ŀ������ؿ�����ʳ���εļӵ����Ϊ��ɫ���ɫ�������ĩ״�ᾧ ��������560�� ��ʼ�ֽ⣬��һ�ֽ�ǿ����������ˮ��Һ������,�ܽ����0�� ʱΪ4.74g��100�� ʱΪ32.3g�� ��ͼ�����ù��������������Ʊ�����صĹ�ҵ���� :
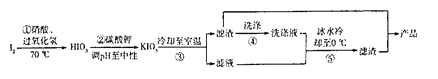
(1)�����������¶���70�� ����,����̫��,���ܵ�ԭ����_______;����̫�� ,ԭ����________________________
(2)д�����������Ҫ��Ӧ�����ӷ���ʽ:__________
(3)������ñ�ˮ��ȴ��0�� ,���˳�����ؾ���,����������ˮϴ��2~3�Ρ��ñ�ˮϴ�ӵ��ŵ���_____________
(4)��Ʒ���Ȳⶨ��ȡ��Ʒ9.0g,������ˮ�ܽⲢ���250mL��Һ��ȡ��25.00mL����Һ����ϡ�����ữ�����������KI��Һ��ʹ����ط�Ӧ��ȫ��������ָʾ���������ʵ���Ũ��Ϊ1.00molL-1��Na2S2O3��Һ�ζ�������25.00mL�õζ�Һʱǡ�ôﵽ�ζ��յ㡣��֪![]()
��ʵ���п���_______��ָʾ����
�ڲ�Ʒ�Ĵ���Ϊ_____%����ȷ��С�������λ������õĴ��ȱ�ʵ��ֵƫ���ܵ�ԭ����________________________��
���𰸡���ֹ���ᡢ��������ֽ� ��Ӧ������ ![]() ����ϴ�ӹ�������ɵ�KIO3��ʧ ���� 99.07 ����ʱ�������������KI���ֱ����������Ʒ�����������ʡ�ȡ�ñ�Һ�ĵζ���û���ñ�Һ��ϴ�Ⱥ����𰸣�
����ϴ�ӹ�������ɵ�KIO3��ʧ ���� 99.07 ����ʱ�������������KI���ֱ����������Ʒ�����������ʡ�ȡ�ñ�Һ�ĵζ���û���ñ�Һ��ϴ�Ⱥ����𰸣�
��������
��1����������������ⲻ�ȶ�������
��2������̼���Ϊ�������Σ�����Ϊǿ��������ӷ���ʽ����д��
��3�����ݵ���ص��ܽ�Ⱥ��¶ȵĹ�ϵ������
��4�����ݷ�Ӧ�й�ϵʽ���м��㡣
(1)����������ⶼ�ֽܷ⣬������Ҫ�����¶ȣ���ֹ���ᡢ��������ֽ⣻�¶���Ӱ�췴Ӧ���ʣ��¶�̫�ͣ���Ӧ��������
(2).̼��غ͵��ᷴӦ���ɵ���غ�ˮ�Ͷ�����̼�����ӷ���ʽΪ��![]() ��
��
(3).�������0�� ʱΪ4.74g��100�� ʱΪ32.3g������Ϊ�˼���ϴ�ӹ�������ɵ�KIO3��ʧ����ʹ�ñ�ˮϴ�ӣ�
(4). ����Ϊ��Ӧ�������еⵥ�����ɣ����õ���������������ԣ�ѡ�������ָʾ����
�� ���ݷ�Ӧ�г���ϵʽΪIO3----6S2O32-������ص���������Ϊ![]() =99.07%������ʱ�������������KI���ֱ����������������Ҫ���������Ƶ������࣬����Ϊ��Ʒ����������������������ĵ����ӣ�������ĵ��������Ƶ������࣬��ȡ�ñ�Һ�ĵζ���û���ñ�Һ��ϴ����Һ������仯�ȡ�
=99.07%������ʱ�������������KI���ֱ����������������Ҫ���������Ƶ������࣬����Ϊ��Ʒ����������������������ĵ����ӣ�������ĵ��������Ƶ������࣬��ȡ�ñ�Һ�ĵζ���û���ñ�Һ��ϴ����Һ������仯�ȡ�

����Ŀ���⼰�仯����������������Ӧ�ù㷺���ش���������:
��1�����ʵ������Ӧ�ɵ�IF5��ʵ�����Һ̬IF5����һ���ĵ�����ԭ������IF5����ż���루��:2H2O![]() H3O++OH-����IF5����ż���뷽��ʽΪ_________
H3O++OH-����IF5����ż���뷽��ʽΪ_________
��2���������ƺ͵������������Һ�еķ�Ӧ��:Na2SO3+KIO3+H2SO4 ��Na2SO4+K2SO4+I2+H2O��δ��ƽ���÷�Ӧ���̺ͻ����ϸ��ӣ�һ����Ϊ��Ϊ���²�:
��IO3-+SO32-��IO2-+SO42-������
��IO2-+SO32-��IO-+SO42-���죩
��5I-+6H++I03-��3I2+3H2O���죩
��I2+SO32-+H2O-��2I+SO42-+2H+���죩
�������������Ʋ⣬�˷�Ӧ���ܷ�Ӧ������_______����Ӧ����������ţ�����Ԥ�ȼ��˵�����Һ��������������_____________����������ʱ���Ż��е��۱��������������
��3�����ӵ���������Ҫ���о�����
����֪SO2��I2�ķ�Ӧ�����ʼ�����ƽ�ⳣ������Һ�д�������ƽ��:I2(aq)+l-(aq)=l3-(aq)�ֽ�1 mol SO2��ͨ�뺬1mol l2��ˮ��Һ����ǡ����ȫ��Ӧ��Һ��l3-�����ʵ���n(l3-)ʱ�䣨t���ı仯������ͼ1��ʾ����ʼ�Σ�n(l3-)�������ԭ����_____
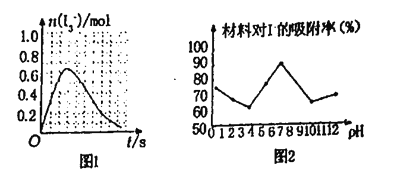
�ڿ���С�������Ͳ���Ag/TiO2����Һ�е����ӽ��������о�����ͼ2�Dz�ͬpH�����£�����������Ч���ı仯���ߡ��ݴ��ƶ�Ag/TiO2�������ʺ�����___________����������������������������������Һ�е�I-��
���Ȼ�������������Ҳ����Ч�����������Ȼ��������������Ե����ӵ�������ӦΪ:I-(aq)+AgCl(s)=Agl(s)+Cl-(aq)����Ӧ�ﵽƽ�����Һ��c(Cl-)=1.0mol��L-1.����Һ��c(I-)=______mol��L-1��k(AgCl)=2.0��10-10��k(Agl)=8.4��10-17��
��4��Fe3+��I-����Һ�з�����Ӧ:2Fe3++2I- ![]() 2Fe2++I2���÷�Ӧ������Ӧ���ʺ�Fe2+��I-��Ũ�ȹ�ϵΪv=k��cm(I-)��cn(Fe3+)������kΪ��������T��ʱ��ʵ����c��I-����c��Fe3+���뷴Ӧ���ʵĹ�ϵ���±���
2Fe2++I2���÷�Ӧ������Ӧ���ʺ�Fe2+��I-��Ũ�ȹ�ϵΪv=k��cm(I-)��cn(Fe3+)������kΪ��������T��ʱ��ʵ����c��I-����c��Fe3+���뷴Ӧ���ʵĹ�ϵ���±���
c��I-��/molL-1 | c��Fe3+��/molL-1 | v/molL-1s-1 | |
�� | 0.20 | 0.80 | 0.032k |
�� | 0.60 | 0.40 | 0.144k |
�� | 0.80 | 0.20 | 0.128k |
����v=k��cm(I-)��cn(Fe3+)��m��n��ֵΪ_____________������ţ�
A.m=1n=1 B.m=1��n=2 C.m=2��n=1 D.m=2��n=2
��I-Ũ�ȶԷ�Ӧ���ʵ�Ӱ��_____����������������С����������������Fe3+Ũ�ȶԷ�Ӧ���ʵ�Ӱ�졣