题目内容
【题目】沐舒坦在临床上广泛使用,合成路线如下(反应试剂和反应条件均末标出)

已知: 
完成下列填空:
(1)写出反应①所用试剂和反应条件_____________
(2)写出反应类型: 反应③____________反应,⑤__________
(3)写出结构简式A________ B__________
(4)反应⑥中除加入反应试剂C外,还需要加入K2CO3,其目的是为了_________;
(5)写出两种C的能发生水解反应,且只含3种不同化学环境氢原子的同分异构体的结构简式_______、__________。
(6)反应②,反应③的顺序不能颠倒,其原因是________________________。
(7)写出反应⑥的化学反应方程式___________。
【答案】 浓硝酸,浓硫酸,水浴加热 还原反应 取代反应 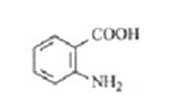
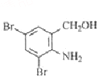 除去生成的HCl,使平衡正向移动,防止产品不纯 (CH3)3CCONHCH3 CH3CONHC(CH3)3 高锰酸钾氧化甲基的同时,也将氨基氧化、最终得不到A
除去生成的HCl,使平衡正向移动,防止产品不纯 (CH3)3CCONHCH3 CH3CONHC(CH3)3 高锰酸钾氧化甲基的同时,也将氨基氧化、最终得不到A 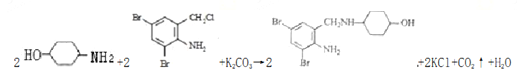
【解析】本题主要考查有机物的结构与性质。
(1)反应①是甲苯的硝化反应,所用试剂和反应条件:浓硝酸,浓硫酸,水浴加热。
(2)反应③硝基还原为氨基,反应类型为还原反应,反应⑤为溴代反应或酯化反应,反应类型为取代反应。
(3结构简式A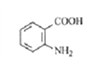 ,B
,B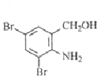 。
。
(4)反应⑥中除加入反应试剂C外,还需要加入K2CO3,其目的是为了除去生成的HCl,使平衡正向移动,防止产品不纯。
(5)C的分子式为C6H13ON,Ω=1,该同分异构体发生水解反应,要求含有肽键—CONH—,且只含3种不同化学环境氢原子,该同分异构体的两种结构简式为(CH3)3CCONHCH3、CH3CONHC(CH3)3。
(6)反应②,反应③的顺序不能颠倒,其原因是高锰酸钾氧化甲基的同时,也将氨基氧化、最终得不到A。
(7)反应⑥的化学方程式: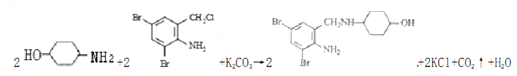 。
。