题目内容
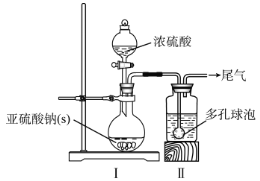
【题目】实验室用如图装置制取少量溴苯,试填写下列空白。

(1)在烧瓶a中装的试剂是铁粉、______和_____。
(2)请你推测长直导管b的作用:__。
(3)请你分析导管c的下口可否浸没于液面中_____?为什么?_____。
(4)反应完毕后,向锥形瓶d中滴加AgNO3溶液有_____生成,此现象说明这种获得溴苯的反应属于_____。(填有机反应类型)
【答案】苯 Br2 导气冷凝和回流 不能 HBr易溶于水很容易倒吸 淡黄色沉淀 取代反应
【解析】
实验室利用苯与液溴在铁做催化剂条件下发生取代反应制取溴苯,溴易挥发长导管可以冷凝回流溴,提高利用率,锥形瓶内盛放硝酸银溶液可以检验是否有HBr生成。
(1)苯与液溴在铁做催化剂条件下发生取代反应,所以在烧瓶a中装的试剂是铁粉、苯、液溴;
(2)溴易挥发,所以长导管的作用除了导气外可以使挥发的溴冷凝回流;
(3)溴化氢易溶于水容易发生倒吸,所以导管c的下口不能浸没于液面中;
(4)溴化氢与硝酸银发生反应生成浅黄色的溴化银沉淀,此现象说明这种获得溴苯的反应属于取代反应。

 阅读快车系列答案
阅读快车系列答案【题目】高炉炼铁过程中发生反应: ![]() Fe2O3(s)+CO(g)
Fe2O3(s)+CO(g)![]()
![]() Fe(s)+CO2(g),该反应在不同温度下的平衡常数见右表。下列说法正确的是( )
Fe(s)+CO2(g),该反应在不同温度下的平衡常数见右表。下列说法正确的是( )
温度T/℃ | 1000 | 1150 | 1300 |
平衡常数K | 4.0 | 3.7 | 3.5 |
A. 由表中数据可判断该反应:反应物的总能量<生成物的总能量
B. 1000℃下Fe2O3与CO反应,t min达到平衡时c(CO) =2×10-3 mol/L,则用CO2表示该反应的平均速率为2×10-3/t mol·L-1·min-1
C. 为了使该反应的K增大,可以在其他条件不变时,增大c(CO)
D. 其他条件不变时,增加Fe2O3的用量,不能有效降低炼铁尾气中CO的含量