题目内容
14.下列说法正确的是( )| A. | 在同温同压下,22.4L的任何气体都是1 mol | |
| B. | 1molCaCl2完全溶于水后,可以得到1 mol Ca2+和2 mol Cl- | |
| C. | 在标准状况下,11.2 L某气体的质量为22 g,则该气体的相对分子质量是44 g/mol | |
| D. | 将80g NaOH固体溶于1 L水中,所得溶液中NaOH的物质的量浓度是2 mol/L |
分析 A.同温同压下,气体摩尔体积相等,但22.4L的任何气体物质的量不一定是1 mol;
B.氯化钙是强电解质,在水溶液中完全电离生成钙离子和氯离子;
C.相对分子质量单位是“1”,摩尔质量单位是g/mol;
D.80gNaOH的物质的量=$\frac{80g}{40g/mol}$=2mol,溶于1L水导致溶液体积大于1L,根据C=$\frac{n}{V}$判断.
解答 解:A.同温同压下,气体摩尔体积相等,气体摩尔体积不一定是22.4L/mol,则22.4L的任何气体物质的量不一定是1 mol,故A错误;
B.氯化钙是强电解质,在水溶液中完全电离生成钙离子和氯离子,根据原子守恒知,1molCaCl2完全溶于水后,可以得到1 mol Ca2+和2 mol Cl-,故B正确;
C.相对分子质量单位是“1”,摩尔质量单位是g/mol,标况下气体摩尔体积是22.4L/mol,则11.2L气体物质的量是0.5mol,其摩尔质量=$\frac{22g}{0.5mol}$=44g/mol,其相对分子质量是44,故C错误;
D.80gNaOH的物质的量=$\frac{80g}{40g/mol}$=2mol,溶于1L水导致溶液体积大于1L,根据C=$\frac{n}{V}$知,其物质的量浓度小于2mol/L,故D错误;
故选B.
点评 本题考查物质的量有关计算,为高频考点,明确物质的量公式中各个物理量关系即可解答,熟练掌握物质的量有关公式,注意C=$\frac{n}{V}$中V指溶液体积而不是溶剂体积,为易错点.

练习册系列答案
相关题目
4.在容积可变的密闭容器中,2molN2和8molH2在一定条件下反应,达到平衡时,H2的转化率为25%,则平衡时氨气的体积分数接近于( )
| A. | 5% | B. | 10% | C. | 15% | D. | 20% |
5.如图所示的家庭小实验中,主要发生物理变化的是( )
| A. | 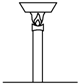 生成炭黑的实验 | B. |  净水 | ||
| C. | 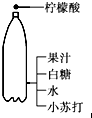 自制汽水 | D. | 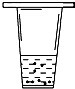 将鸡蛋壳放入醋中 |
2.恒温下,下列情景中最终不能析出固体的是( )
| A. | 将CO2持续通入NaCl和NH3均达饱和的混合溶液中 | |
| B. | 将CO2持续通入饱和Na2CO3溶液中 | |
| C. | 将少量SO2通入NH3和BaCl2的混合溶液中 | |
| D. | 将NH3持续通入AgNO3溶液中 |
9.下列物质中,分子数目最多的是( )
| A. | 2molCl2 | B. | 3.01×1023个氧分子 | ||
| C. | 2g氢气 | D. | 标准状况下,11.2LHe |
19.设NA代表阿伏加德罗常数的值,下列说法正确的是( )
| A. | 15.6g Na2O2与足量二氧化碳反应,转移的电子总数为0.2 NA (2 Na2O2+2CO2=2Na2CO3+O2) | |
| B. | 标准状况下,22.4L CCl4中含有的C原子数目为NA | |
| C. | 常温常压下,0.84g NaHCO3含有的Na+离子数为0.01 NA | |
| D. | 物质的量浓度为0.5 mol•L-1的MgCl2溶液中,所含Cl-个数为NA |