题目内容
在元素周期表中金属元素和非金属元素分界线附近,容易找到的元素是( )
| A、耐高温的合金材料 |
| B、制农药的元素 |
| C、作半导体材料的元素 |
| D、作催化剂的元素 |
考点:元素周期表的结构及其应用
专题:
分析:在金属元素与非金属元素的分界线附近的元素,通常既具有金属性又具有非金属性,可以找到半导体材料.
解答:
解:A.耐高温的合金材料在过渡元素区寻找,故A不选;
B.制农药的元素在周期表右上方的非金属元素区寻找,故B不选;
C.作半导体材料的元素,在元素周期表金属元素与非金属元素的分界线附近寻找,故C选;
D.做催化剂的元素从过渡元素区寻找,故D不选.
故选C.
B.制农药的元素在周期表右上方的非金属元素区寻找,故B不选;
C.作半导体材料的元素,在元素周期表金属元素与非金属元素的分界线附近寻找,故C选;
D.做催化剂的元素从过渡元素区寻找,故D不选.
故选C.
点评:本题考查元素周期表的结构及应用,为高频考点,把握元素的位置及性质为解答的关键,注重基础知识的考查,题目难度不大.

练习册系列答案
相关题目
关于实验室制取乙烯的实验,下列说法正确的是( )
| A、所用的反应药品为1体积酒精和3体积浓度为5mol/L的硫酸 |
| B、反应容器(烧瓶)中应加入少许碎瓷片 |
| C、温度计要插入反应液体的液面下,以控制温度在140℃ |
| D、收集乙烯可用排水法,也可用排空气法 |
在容积固定的密闭容器中充入一定量的X、Y两种气体,一定条件下发生可逆反应3X(g)+Y(g)═2Z(g),并达到平衡.已知正反应是放热反应,测得X的转化率为37.5%,Y的转化率为25%,下列有关叙述正确的是( )
| A、若X的反应速率为0.2 mol?L-1?s-1,则Z的反应速率为0.3 mol?L-1?s-1 |
| B、若向容器中充入氦气,压强增大,Y的转化率提高 |
| C、升高温度,正反应速率减小,平衡向逆反应方向移动 |
| D、开始充入容器中的X、Y物质的量之比为2:1 |
如图为铜-锌-稀硫酸构成的原电池示意图,下列说法错误的是( )
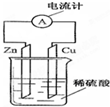

| A、负极反应式为:Zn-2e-═Zn2+ |
| B、正极反应式为:2H++2e-═H2↑ |
| C、电子由锌片通过导线流向铜片,再由铜片经电解质溶液流回锌片 |
| D、该装置能将化学能转变为电能 |
类推的思维方式在化学学习与研究中经常采用,但类推出的结论是否正确最终要经过实验的验证.以下类推的结论正确的是( )
| A、由“Cl2+H2O═HCl+HClO”可推出“F2+H2O═HF+HFO” |
| B、HCl的水溶液是强酸,推出HF的水溶液也是强酸 |
| C、由“2Fe+3Cl2═2FeCl3”可推出“2Fe+3I2═2FeI3” |
| D、Na常温下与水剧烈反应,故K常温下也能与水剧烈反应 |
下列现象因发生加成反应而产生的是( )
| A、乙烯使溴的四氯化碳溶液褪色 |
| B、乙烯使酸性KmnO4溶液褪色 |
| C、甲烷与氯气混合,光照一段时间后黄绿色消失 |
| D、将苯加人溴水中,振荡后水层接近无色 |
下列说法不正确的是( )
| A、苯和浓硫酸在70~80℃时发生磺化反应 | ||
| B、芳香烃是分子组成符合CnH2n-6(n≥6)的一类物质 | ||
| C、甲苯可以和浓硝酸与浓硫酸的混合物发生硝化反应 | ||
D、等质量的烃(CXHY)耗氧量取决于
|
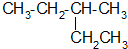 的系统命名为
的系统命名为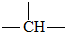 和一个-F,符合此要求的可能结构有
和一个-F,符合此要求的可能结构有