题目内容
【题目】如图所示的各图中,表示2A(g)+B(g)2C(g)(△H<0)这个可逆反应的正确图象为(注:(C)表示C的质量分数,P表示气体压强,C表示浓度)
A.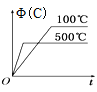 B.
B.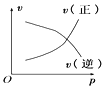 C.
C.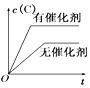 D.
D.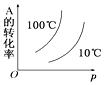
【答案】A
【解析】
A.温度升高,反应速率加快,达到平衡所需的时间缩短,反应逆向移动;
B.增大压强,反应速率加快,平衡向体积缩小的方向移动;
C.加入催化剂,反应速率加快,达到平衡所需的时间缩短,但质量分数不发生变化;
D.降低温度,平衡向放热反应方向移动,增大压强,平衡向体积缩小的方向移动;
A. 温度升高,反应速率加快,达到平衡所需的时间缩短,反应逆向移动,C的质量分数降低,A项正确;
B. 增大压强,反应速率加快,v(正)、v(逆)均增大,B项错误;
C. 加入催化剂,反应速率加快,达到平衡所需的时间缩短,但C的质量分数不发生变化,C项错误;
D. 降低温度,平衡向放热反应方向移动,即正向移动,A的转化率增大;增大压强,平衡向体积缩小的方向移动,即正向移动,A的转化率增大,D错误;
答案选A。
改变的条件(其他条件不变) | 化学平衡移动的方向 | |||
浓度 | 增大反应物浓度或减小生成物浓度 | 向正反应方向移动 | ||
减小反应物浓度或增大生成物浓度 | 向逆反应方向移动 | |||
压强(对有气体参加的反应) | 反应前后气体体积改变 | 增大压强 | 向气体分子总数减小的方向移动 | |
减小压强 | 向气体分子总数增大的方向移动 | |||
反应前后气体体积不变 | 改变压强 | 平衡不移动 | ||
温度 | 升高温度 | 向吸热反应方向移动 | ||
降低温度 | 向放热反应方向移动 | |||
催化剂 | 同等程度改变v正、v逆,平衡不移动 | |||

练习册系列答案
 阅读快车系列答案
阅读快车系列答案
相关题目