题目内容
【题目】有研究表明,内源性H2S作为气体信号分子家族新成员,在抗炎、舒张血管等方面具有重要的生理作用,而笼状COS(羰基硫)分子可作为H2S的新型供体(释放剂)。试回答下列有关问题
(1)COS的分子结构与CO2相似,COS的结构式为______。
(2)已知:①COS(g)+H2(g)H2S(g)+CO(g)△H1=-15kJmol-1,②COS(g)+H2(g)H2S(g)+CO2(g)△H2=-36kJmol-1,③CO(g)+H2O(g)H2(g)+CO2(g)△H3,则△H=______。
(3)COS可由CO和H2S在一定条件下反应制得。在恒容的密闭容器中发生反应并达到平衡:CO(g)+H2S(g)COS(g)+H2(g),数据如表所示、据此填空
实验 | 温度/℃ | 起始时 | 平衡时 | |||
n(CO)/mol | n(H2S)/mol | n(COS)/mol | n(H2)/mol | n(CO)/mol | ||
1 | 150 | 10.0 | 10.0 | 0 | 0 | 7.0 |
2 | 150 | 7.0 | 8.0 | 2.0 | 4.5 | x |
3 | 400 | 20.0 | 20.0 | 0 | 0 | 16.0 |
①该反应为______(选填“吸热反应”或“放热反应”)。
②实验2达到平衡时,x______7.0(选填“>”、“<”或“=”)
③实验3达到平衡时,CO的转化率α=______
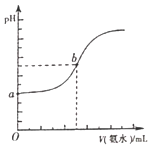
(4)已知常温下,H2S和NH3H2O的电离常数分别为向pH=a的氢硫酸中滴加等浓度的氨水,加入氨水的体积(V)与溶液pH的关系如图所示:
酸/碱 | 电离常数 | |
H2S | Ka1=1.0×10-7 | Ka2=7.0×10-15 |
NH3H2O | Kb=1.0×10-5 | |
①若c(H2S)为0.1mol/L,则a=______
②若b点溶液pH=7,则b点溶液中所有离子浓度大小关系是______。
(5)将H2S通入装有固体FeCl2的真空密闭烧瓶内,恒温至300℃,反应达到平衡时,烧瓶中固体只有FeCl2和FeSx(x并非整数),另有H2S、HCl和H2三种气体,其分压依次为0.30P0、0.80P0和0.04P0(P0表示标准大气压)。当化学方程式中FeCl2的计量数为1时,该反应的气体压强平衡常数记为Kp。计算:
①x=______(保留两位有效数字)。
②Kp=______(数字用指数式表示)。
【答案】O=C=S 21kJmol-1 放热反应 < 20% 4 c(NH4+)>c(HS-)>c(H+)=c(OH-)>c(S2-) 1.1 ![]()
【解析】
(1)CO2和COS是等电子体,等电子体结构相似,根据二氧化碳的分子的结构式可知COS结构式;
(2)根据盖斯定律计算可得;
(3)①分别建立三段式计算实验1和实验3的化学平衡常数,依据平衡常数的大小判断反应时放热还是吸热;
②通过浓度熵与平衡常数的大小判断平衡移动方向;
③依据三段式和转化率公式计算;
(4)①依据电离常数公式计算;
②依据电离程度和水解程度的相对大小判断;
(5)依据题给信息写出反应的化学方程式,由题给数据和公式计算即可。
(1)由二氧化碳分子的结构式可知:COS分子中C与O、C与S均形成两对共有电子对,所以COS结构式为:O=C=S,故答案为:O=C=S;
(2)盖斯定律②-①得到CO(g)+H2O(g)H2(g)+CO2(g)的焓变△H3=-36kJmol-1-(-15kJmol-1)=-21kJmol-1,故答案为:-21kJmol-1;
(3)设容器体积为1L。
①由题意可建立实验1反应的三段式为:
CO(g)+H2S(g)COS(g)+H2(g)
开始(mol/L)10.010.000
反应(mol/L)3.0 3.0 3.0 3.0
平衡(mol/L)7.0 7.0 3.0 3.0
化学平衡常数=![]() =
=![]() =0.18;
=0.18;
由题意可建立实验3反应的三段式为:
CO(g)+H2S(g)COS(g)+H2(g)
开始(mol/L) 20.0 20.0 0 0
反应(mol/L) 4.04.04.0 4.0
平衡(mol/L) 16.016.0 4.0 4.0
化学平衡常数=![]() =
=![]() =0.0625<0.18,所以升高温度,平衡常数k减小,即平衡逆向移动,正向即放热反应,故答案为:放热反应;
=0.0625<0.18,所以升高温度,平衡常数k减小,即平衡逆向移动,正向即放热反应,故答案为:放热反应;
②150℃,浓度熵Qc=![]() =
=![]() ≈0.16<k=0.18,则反应向正反应方向移动,所以实验2达平衡时,n(CO)减小,x<7.0,故答案为:<;
≈0.16<k=0.18,则反应向正反应方向移动,所以实验2达平衡时,n(CO)减小,x<7.0,故答案为:<;
③实验3达平衡时,CO的转化率=![]() ×100%=
×100%=![]() ×100%=20%,故答案为:20%;
×100%=20%,故答案为:20%;
(4)①c(H+)=![]() =
=![]() mol/L=10-4mol/L,a=pH=-lg10-4=4,故答案为:4;
mol/L=10-4mol/L,a=pH=-lg10-4=4,故答案为:4;
②b点呈中性,则c(H+)=c(OH-),溶液中电荷关系为c(NH4+)+c(H+)=c(HS-)+2c(S2-)+c(OH-),所以c(NH4+)>c(HS-),由于HS-的电离程度很小、主要以电离为主,同时促进水的电离,所以c(H+)>c(S2-),即b点时溶液中所有离子浓度大小关系是c(NH4+)>c(HS-)>c(H+)=c(OH-)>c(S2-),故答案为:c(NH4+)>c(HS-)>c(H+)=c(OH-)>c(S2-);
(5)H2S和FeCl2反应的方程式为xH2S(g)+FeCl2(s)FeSx(s)+2HCl(g)+(x-1)H2(g)。
①有化学方程式可得关系式:2:(x-1)=0.80P0:0.04P0,解得x=1.1,故答案为:1.1;
②H2S和FeCl2反应的方程式为1.1H2S(g)+FeCl2(s)FeS1.1(s)+2HCl(g)+0.1H2(g),由方程式可得p(HCl)=0.80P0,p(H2)=0.04P0,p(H2S)=0.30P0,平衡分压常数Kp=![]() /span>
/span>
=![]() ,故答案为:
,故答案为:![]() 。
。